Pain Modulation Pathway Mechanisms i El Paso, TX
De fleste, hvis ikke alle, lidelser i kroppen udløser smerter. Smerte fortolkes og sanses i hjernen. Smerte moduleres af to nøgletyper af lægemidler, der virker på hjernen: analgetika og anæstetika. Udtrykket analgetikum refererer til en medicin, der lindrer smerter uden tab af bevidsthed. Udtrykket central anæstesi refererer til en medicin, der deprimerer CNS. Det er kendetegnet ved manglen på al opfattelse af sensoriske modaliteter, for eksempel tab af bevidsthed uden tab af kritiske funktioner.
Opiatanalgesi (OA)
De mest succesrige klinisk anvendte lægemidler til at producere midlertidig analgesi og lindring af smerte er opioidfamilien, som omfatter morfin og heroin. Der er i øjeblikket ingen yderligere kraftfulde smerteterapeutiske muligheder for opiater. Adskillige bivirkninger forårsaget af opiatbrug omfatter tolerance og stofafhængighed eller afhængighed. Generelt modulerer disse lægemidler den indkommende smerteinformation i rygsøjlen og centralnervesystemet, ud over at de lindrer smerte midlertidigt og kan også kaldes opiatproducerende analgesi (OA). Opiatantagonist er et lægemiddel, der modvirker opioidvirkningerne, såsom naloxon eller maltroxon osv.. De er kompetitive antagonister af opiatreceptorer. Imidlertid har hjernen et neuronalt kredsløb og endogene stoffer, som modulerer smerte.
Endogene opioider
Opioidergisk neurotransmission er lokaliseret i hele hjernen og rygmarven og menes at påvirke mange funktioner i centralnervesystemet eller CNS, såsom nociception, kardiovaskulære funktioner, termoregulering, respiration, neuroendokrine funktioner, neuroimmune funktioner, fødevareforbrug, seksuel aktivitet, konkurrencedygtig bevægelsesadfærd samt hukommelse og indlæring. Opioider har en markant effekt på humør og motivation og giver en følelse af eufori.
Tre klasser af opioidreceptorer identificeres: a-mu, a-delta og a-kappa. Alle 3 klasser er vidt spredt i hjernen. Generne, der koder for hver af disse, er blevet klonet og fundet at fungere som medlemmer af G-proteinreceptorerne. Desuden er tre hovedtyper af endogene opioidpeptider, der interagerer med de ovennævnte opiatreceptorer, blevet genkendt i centralnervesystemet, herunder a-endorfiner, enkephaliner og dynorphinerne. Disse 3 opioidpeptider er afledt af en stor proteinreceptor af tre forskellige gener, såsom proopiomelanocortin- eller POMC-genet, proenkephalingenet og prodynorphin-genet.�Opioidpeptiderne modulerer nociceptivt input på to måder: For det første blokerer de neurotransmitter frigivelse ved at hæmme Ca2+-tilstrømning i den præsynaptiske terminal, eller for det andet åbner de kaliumkanaler, som hyperpolariserer neuroner og hæmmer spike-aktivitet. De virker på forskellige receptorer i hjernen og rygmarven.
Enkephaliner betragtes som de formodede ligander for ? receptorer, ? endorfiner for dets a-receptorer og dynorfiner for ? receptorer. De forskellige typer opioidreceptorer er fordelt forskelligt i det perifere og centrale nervesystem eller CNS. Der er beviser for funktionelle forskelle i disse receptorer i forskellige strukturer. Dette forklarer, hvorfor mange uønskede bivirkninger opstår efter opiatbehandlinger. For eksempel er mu (?) receptorer udbredt i hjernestammens parabrachiale kerner, hvor et respirationscenter og hæmning af disse neuroner kan forårsage det, der er kendt som respirationsdepression.
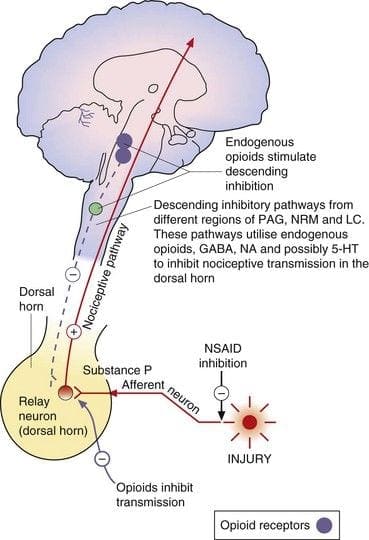
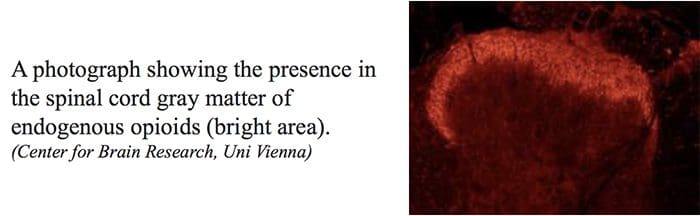
Centrale eller perifere terminaler af nociceptive afferente fibre har opiatreceptorer, hvori eksogene og endogene opioider kan virke for at modulere evnen til at transmittere nociceptiv information. Derudover findes høje tætheder af opiatreceptorer i periaqueductal grå eller PAG, nucleus raphe magnus eller NRM og dorsal raphe eller DR fra den rostrale ventrale medulla, i rygmarven, caudate nucleus eller CN, septal nucleus, hypothalamus, habenula og hippocampus.�Systemisk administrerede opioider i analgetiske doser aktiverer spinale og supraspinale mekanismer via ?, ?, og ? type opioidreceptorer og regulere smertesignaler for at modulere symptomer.
Neuronale kredsløb og smertemodulering
I mange årtier blev det foreslået, at der et sted i centralnervesystemet er et kredsløb, som kan modulere indkommende smertedetaljer. Gatekontrolteorien og det stigende/faldende smertetransmissionssystem er to forslag til et sådant kredsløb. Nedenfor vil vi diskutere begge dele mere detaljeret.
Gate kontrol teori
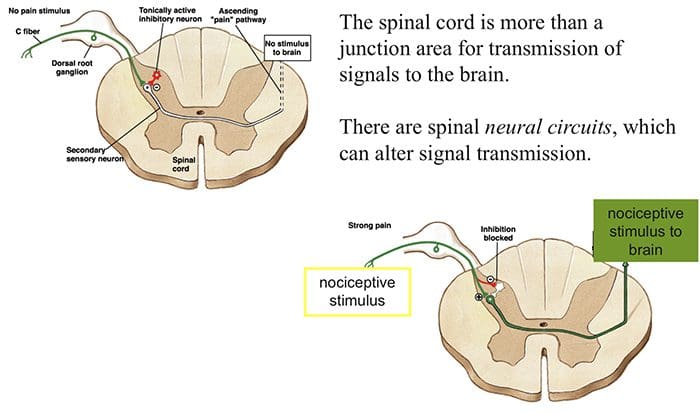
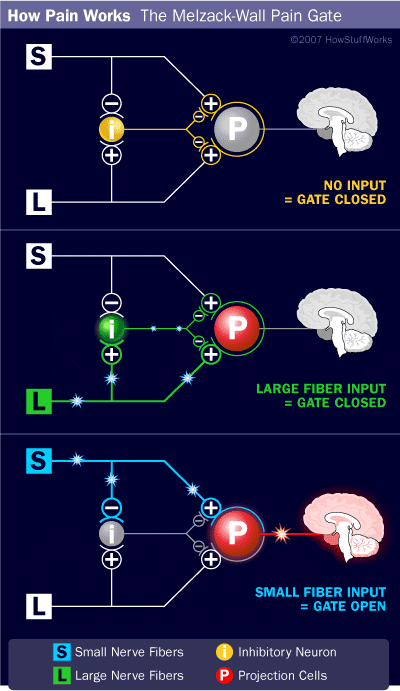
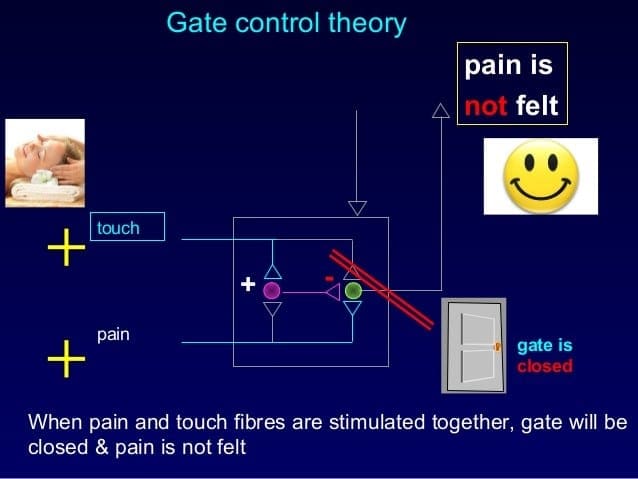
Den indledende smertemodulerende mekanisme kendt som gate kontrol teori, er blevet foreslået af Melzack og Wall i midten af 1960'erne. Forestillingen om gatekontrolteorien er, at ikke-smertefuldt input lukker portene for smertefuldt input, hvilket resulterer i, at man undgår smertefornemmelsen fra rejse ind i CNS, for eksempel undertrykker ikke-skadende input eller stimulation smerte.
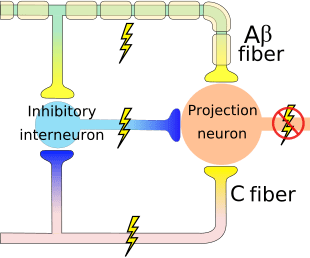
Teorien antyder, at collateraler af de store sensoriske fibre, der bærer kutane sensoriske input, aktiverer hæmmende interneuroner, som hæmmer og regulerer smertetransmissionsdata fra smertefibrene. Ikke-skadeligt input hæmmer smerte eller sensorisk input og lukker porten for skadeligt input. Gatekontrolteorien viser, at i rygmarvsniveauet vil ikke-skadelig stimulering skabe præsynaptisk hæmning på dorsale rodnociceptorfibre, der synapser på nociceptorernes spinale neuroner (T). Denne præsynaptiske hæmning vil også forhindre indgående skadelig information i at nå CNS, for eksempel vil den lukke porten til indgående toksisk information.
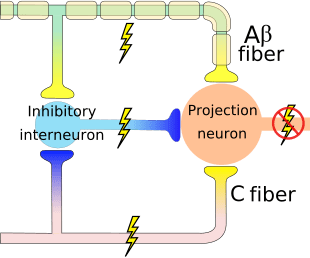
Gatekontrolteorien var begrundelsen for ideen bag produktionen og udnyttelsen af den transkutane elektriske nervestimulation, eller TENS, til smertelindring. For at være effektiv genererer TENS-enheden to forskellige nuværende frekvenser under den smertetærskel, som patienten kan tage. Denne proces har fundet en grad af præstation i kronisk smertebehandling.
Smertemodulation: Gate Control Theory
Stimuleringsfremkaldt analgesi (SPA)
Beviser for et iboende analgesisystem blev fundet ved intrakraniel elektrisk stimulering af visse diskrete hjerneområder. Disse områder ville være den periaqueductal grå eller PAG og nucleus raphe magnus eller NRM, dorsal raphe eller DR, caudate nucleus eller CN, septal nucleus eller Spt sammen med andre kerner. Sådanne stimuleringer eller sensoriske signaler hæmmer smerte, hvilket gør analgesi uden adfærdsundertrykkelse, mens berørings-, temperatur- og trykfornemmelsen forbliver intakt. Ifølge forskningsundersøgelser er SPA, eller stimulation produceret analgesi, mere udtalt og fortsætter i længere tid efter stimulation hos mennesker end hos forsøgsdyr. Under SPA reagerer forsøgspersonerne dog stadig på ikke-smertefuld stimulering som temperatur og berøring inden for det afgrænsede område af analgesi. De mest effektive CNS- eller centralnervesystemregioner for at SPA kan forekomme, ville være i PAG'en og raphe-kernerne eller RN.
Elektrisk stimulering af PAG eller NRM hæmmer spinale thalamusceller eller spinale neuroner, der projicerer monosynaptisk til thalamus, i laminae I, II og V for at sikre den skadelige information fra nociceptorerne, som i sidste ende moduleres i niveauet af rygmarven. Desuden har PAG neuronale forbindelser til nucleus raphe magnus eller NRM.
Aktiviteten af PAG forekommer højst sandsynligt ved aktivering af den nedadgående vej fra NRM og sandsynligvis også ved aktivering af stigende forbindelser, der virker på større subkortikale niveauer af CNS. Derudover producerer elektrisk stimulering af PAG eller NRM adfærdsmæssige analgesi, eller stimulering produceret analgesi. Stimulering frembragte analgesi eller SPA forårsager frigivelse af endorfiner, som kan blokeres af opiatantagonisten naloxon.
Under PAG- og/eller RN-stimulering kan serotonin, også medicinsk benævnt 5-HT, også udledes fra opstigende og nedadgående axoner fra subkortikale kerner, i rygmarvs trigeminuskerner og i rygmarven. Denne frigivelse af 5-HT modulerer og regulerer smertetransmission ved at hæmme eller blokere indkommende neurale handlinger. Udtømning af 5-HT ved elektrisk læsion af raphe-kernerne eller med en neurotoksisk læsion fremstillet ved lokal injektion af et kemisk middel såsom parachlorphenylalanin eller PCPA, resulterer i blokering af opiatets kraft, både intrakraniel og systemisk, såvel som elektrisk stimulering for at frembringe analgesi.
For at bekræfte, om den elektriske stimulation gav analgesi via frigivelsen af opiat og dopamin, mikroinjiceres regionen lokalt med morfin eller 5-HT. Alle disse mikroinjektioner skaber i sidste ende analgesi. Disse processer giver også en måde at identificere hjerneområder relateret til smerteundertrykkelse og hjælpe med at producere et kort over smertecentre. Den mest effektive måde at producere opiat-analgesi, eller OA, er ved intracerebral injektion af morfin i PAG.
PAG og RN samt andre hjernestrukturer, hvori analgesi produceres, er også rige på opiatreceptorer. Intracerebral opioidadministration frembragte analgesi og SPA kan blokeres af systemisk eller fra lokale mikroinjektioner af naloxon, morfinantagonisten, i PAG eller RN. Af den grund er det blevet foreslået, at de to, både OA og SPA, fungerer ved en hyppig mekanisme.
Hvis OA og SPA opfører sig gennem det samme iboende system, så er hypotesen om, at opiater aktiverer en smertedæmpende mekanisme, meget mere sandsynlig. Faktisk tyder aktuelle beviser på, at mikroinjektioner af et opiat i PAG aktiverer et efferent hjernestammesystem, som hæmmer smertetransmission ved segmentelle rygmarvsniveauer. Disse observationer indebærer, at analgesi fremkaldt fra den periaqueductal grå, eller PAG, kræver en nedadgående vej ind i rygmarven.

Dr. Alex Jimenez's Insight
Smertemodulation sker gennem processen med elektrisk hjernestimulering, som opstår på grund af aktiveringen af nedadgående hæmmende fibre, som regulerer eller hæmmer input og output fra visse neuroner. Det, der er blevet beskrevet som opioid- og serotonerge antagonister, menes at vende både lokal opiat-analgesi og hjernestimuli-genereret analgesi. De sensoriske signaler eller impulser i centralnervesystemet styres i sidste ende af både stigende og faldende hæmmende systemer, ved at anvende endogene opioider eller andre endogene stoffer, såsom serotonin som hæmmende mediatorer. Smerte er en kompleks opfattelse, som også kan påvirkes af en række andre faktorer, herunder følelsesmæssig tilstand.
Mekanismer for smertemodulering
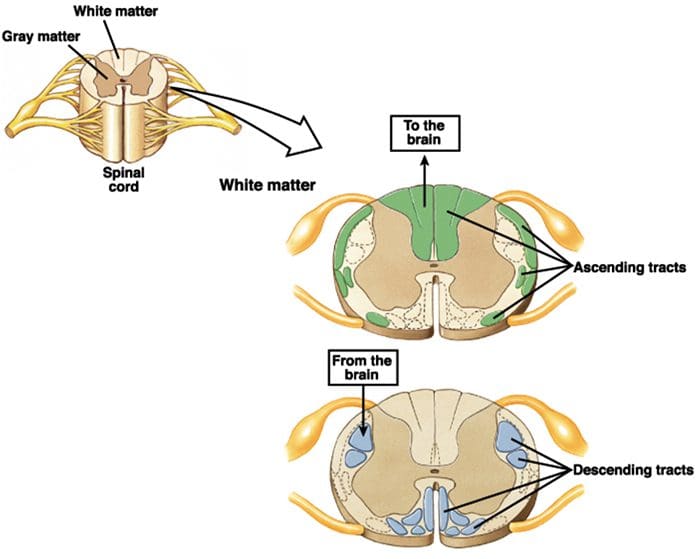
Stigende og faldende smertedæmpningsmekanisme
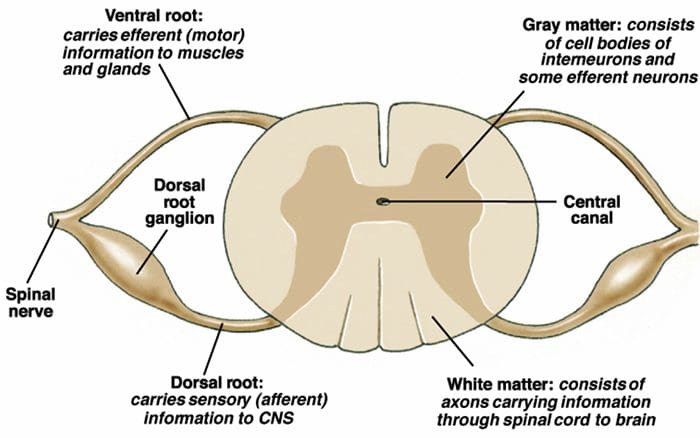
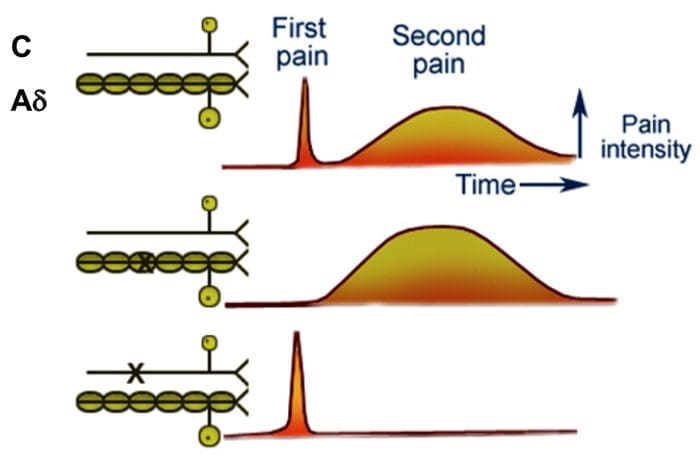
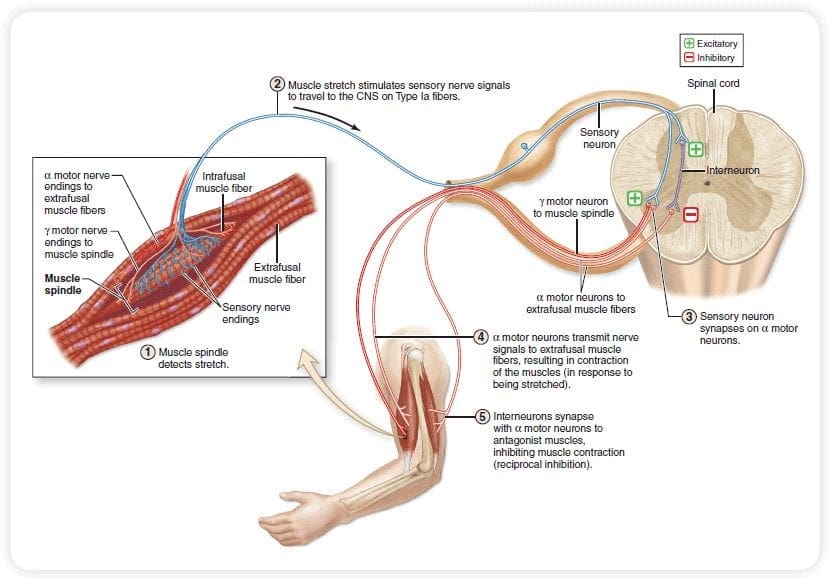
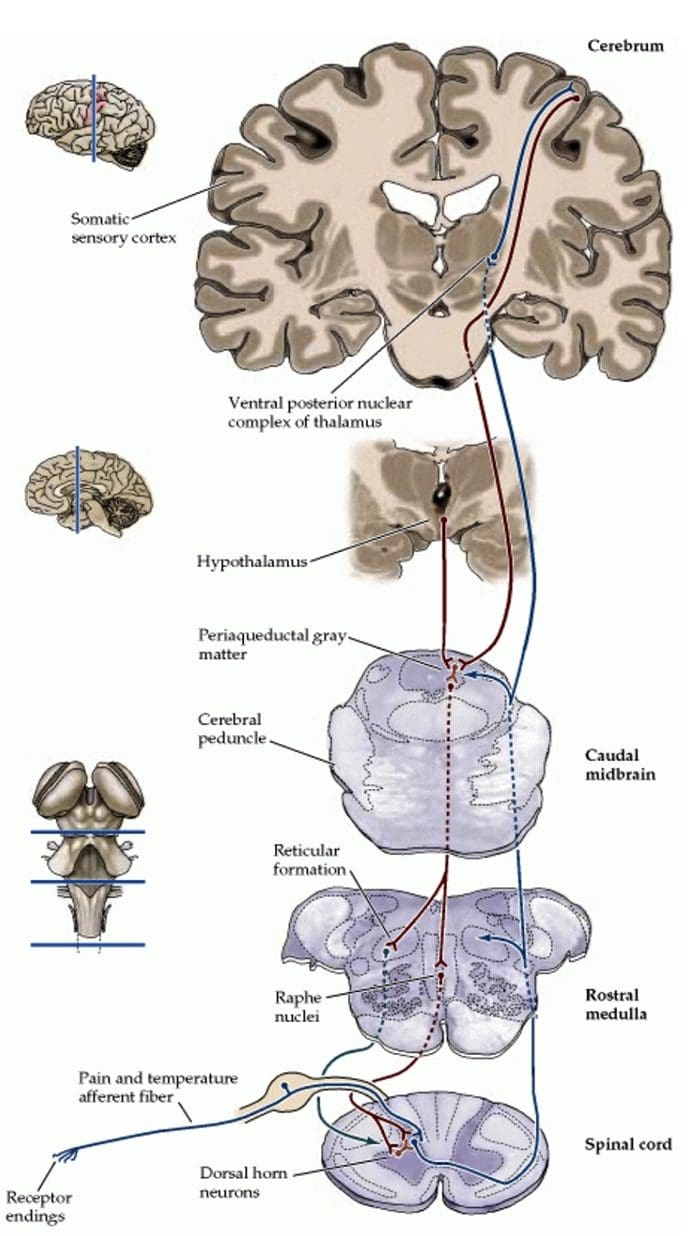
De primære opstigende smertefibre, såsom A ? og C-fibre, når rygmarvens dorsale horn fra perifere nerveområder for at innervere nociceptorneuronerne i Rexed laminae I & II. Celler fra Rexed lamina II laver synaptiske forbindelser i Rexed lag IV til VII. Celler, især inden for laminae I og VII af det dorsale horn, giver anledning til stigende spinothalamiske kanaler. I det spinale niveau er opiatreceptorer placeret i de præsynaptiske ender af deres nocineuroner og i de interneurale niveaulag IV til VII fra det dorsale horn.
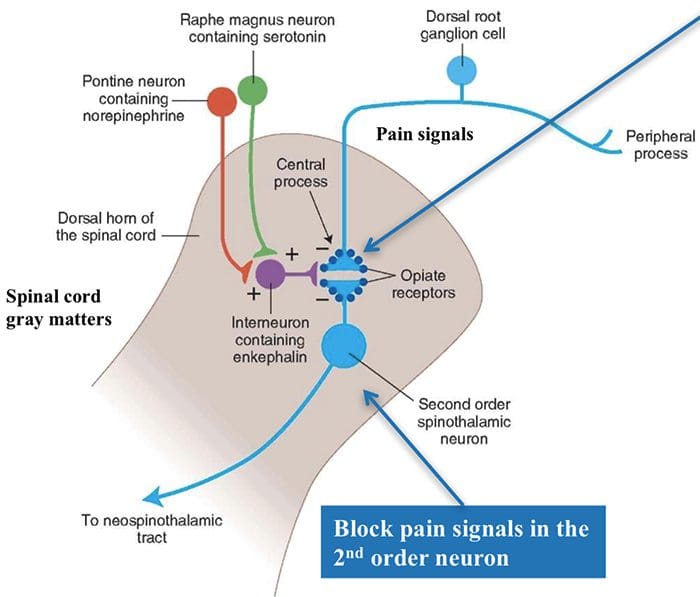
Aktivering af opiatreceptorer på det interneuronale niveau frembringer hyperpolarisering af neuronerne, hvilket fører til hæmning af aktivering samt frigivelse af substans P, en neurotransmitter involveret i smerteoverførsel, og dermed forhindrer smerteoverførsel. Kredsløbet, som består af det periaqueductale grå eller PAG, stof i den øvre hjernestamme, locus coeruleus eller LC, nucleus raphe magnus eller NRM og nucleus reticularis gigantocellularis eller Rgc fører til den faldende smerte suppression pathway, som hæmmer indkommende smertedata på rygmarvsniveau.
Som nævnt før interagerer opioider med opiatreceptorerne i forskellige centralnervesystemniveauer. Disse opiatreceptorer er de normale målområder for hormoner og endogene opiater, såsom endorfinerne og enkephalinerne. På grund af binding til receptoren i subkortikale websteder, sekundære ændringer, som resulterer i nogle ændringer i neuronernes elektrofysiologiske egenskaber og regulering af deres stigende smerteinformation.
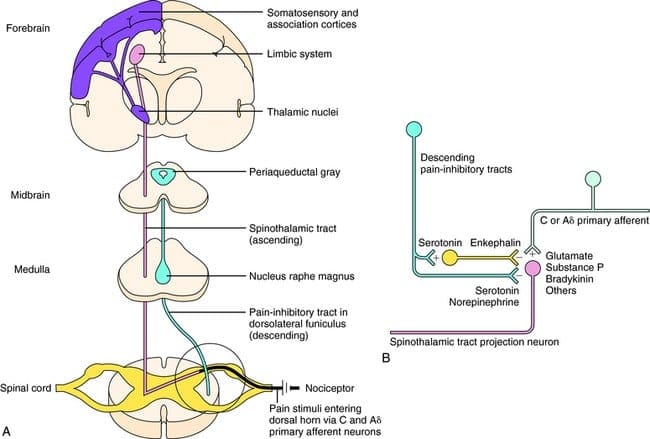
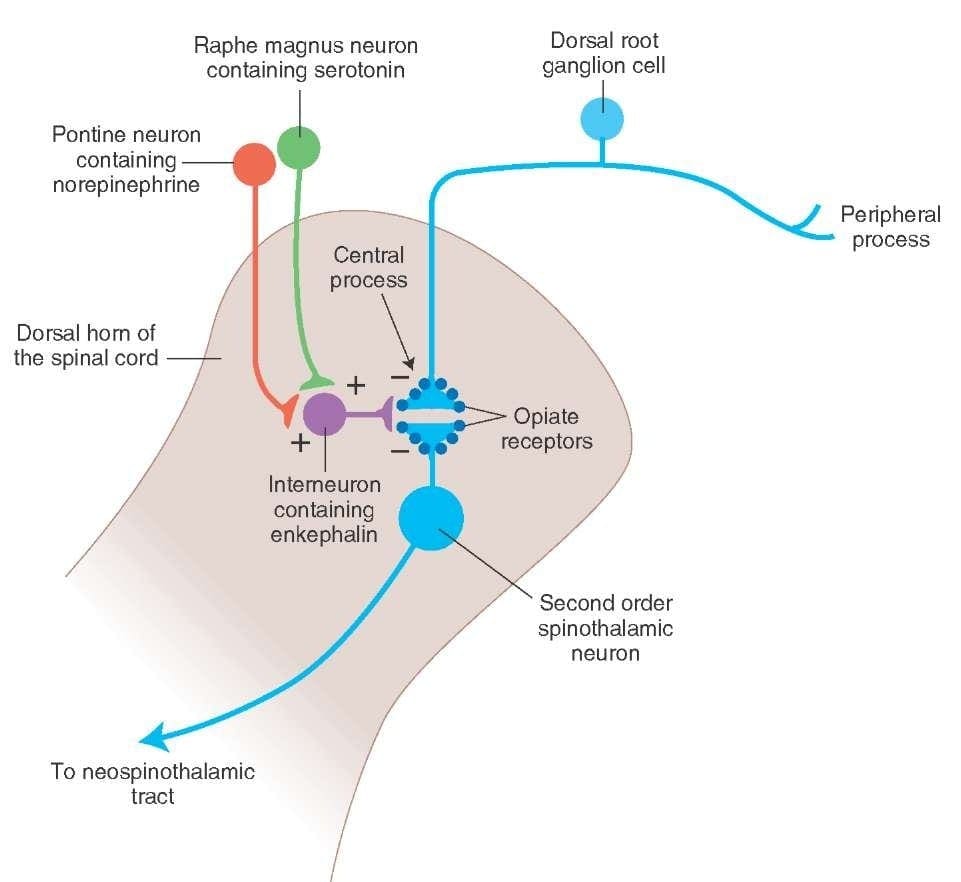
Hvad aktiverer PAG til at udøve sine konsekvenser? Det blev opdaget, at skadelig stimulation udløser neuroner i nucleus reticularis gigantocellularis eller RGC. Kernen Rgc innerverer både PAG og NRM. PAG'en sender axoner ind i NRM, og nerver i NRM sender deres axoner til rygmarven. Derudover blokerer bilaterale dorsolaterale funiculus, eller DLF, læsioner, refereret til som DLFX, analgesien produceret af både elektrisk stimulering og ved mikroinjektion af opiater direkte i PAG og NRM, men de dæmper blot de systemiske analgetiske virkninger af opiater. Disse observationer understøtter hypotesen om, at diskrete faldende veje fra DLF er nødvendige for både OA og SPA.
DLF består af fibre, der stammer fra flere hjernestammekerner, som kan være serotonerge eller 5-HT, fra nerver placeret inde i nucleus raphe magnus eller NRM; dopaminerge neuroner, der stammer fra det ventrale tegmentale område, eller VTA, og adrenerge neuroner, der stammer fra locus coeruleus eller LC. Disse nedadgående fibre undertrykker skadelig input i de nociceptive rygmarvsneuroner i laminae I, II og V.
Opiatreceptorer er også blevet opdaget i rygmarvens dorsale horn, hovedsageligt i Rexed laminae I, II og V, og sådanne spinale opiatreceptorer medierer hæmmende virkninger på dorsale hornneuroner, der transmitterer nociceptiv information. Virkningen af morfin synes at blive udøvet ligeligt i rygmarven og hjernestammen, inklusive PAG og NRM. Systemisk morfin virker på både hjernestamme- og rygmarvsopiatreceptorer og producerer analgesi. Morfin binder hjernestammens opiatreceptorer, hvilket udløser hjernestammens serotonerge vej ned i rygmarven samt DLF, og disse har en opioid-medieret synapse på rygmarvsniveau.
Denne observation viser, at skadelige stimuli, i stedet for ikke-skadelige stimuli, bestemmer gatekontrolteorien, som er kritiske for aktiveringen af det faldende smertemodulationskredsløb, hvor smerte hæmmer smerte via den faldende DLF-vej. Derudover er der stigende forbindelser i PAG og raphe kernerne ind i PF-CM komplekset. Disse thalamiske regioner er en del af den stigende smertemodulation ved diencephalon-graden.
Stressinduceret analgesi (SIA)
Analgesi kan opstå under visse stressende omstændigheder. Udsættelse for mange forskellige stressende eller smertefulde hændelser genererer en smertestillende reaktion. Dette fænomen er kendt som stressinduceret analgesi eller SIA. Stressinduceret analgesi er blevet antaget at give indsigt i de fysiologiske og psykologiske faktorer, der udløser endogen smertekontrol og opiatsystemer. For eksempel rapporterer soldater, der er såret i kamp, eller atleter, der er kommet til skade i sport, nogle gange, at de ikke føler smerte eller ubehag under kampen eller kampen, ikke desto mindre vil de gå igennem smerten bagefter, når den specifikke situation er stoppet. Det er blevet påvist hos dyr, at elektriske stød forårsager stress-induceret analgesi. På baggrund af disse eksperimenter antages det, at det pres, soldaterne og atleterne oplevede, undertrykte den smerte, som de senere ville opleve.
Det menes, at endogene opiater produceres som reaktion på stress og hæmmer smerter ved at udløse det nedadgående system i mellemhjernen. Desuden udviste nogle SIA krydstolerance med opiat-analgesi, hvilket indikerer, at denne SIA er medieret via opiatreceptorer. Eksperimenter, der anvender forskellige parametre for elektrisk stødstimulering, viser en sådan stressinduceret analgesi, og nogle af de bekymringer, der producerer analgesi, kunne blokeres af opioidantagonisten naloxon, mens andre ikke blev blokeret af naloxon. Som konklusion fører disse bemærkninger til beslutningen om, at der findes både opiat- og ikke-opiatformer for SIA.
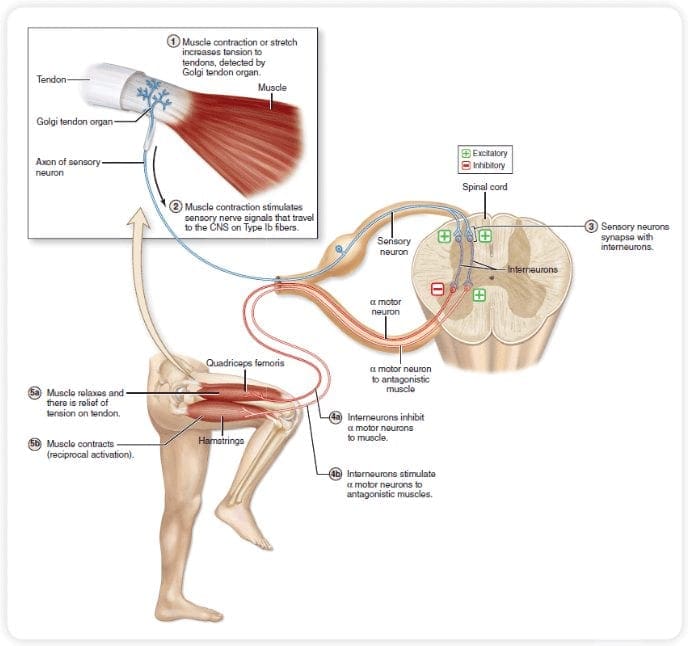
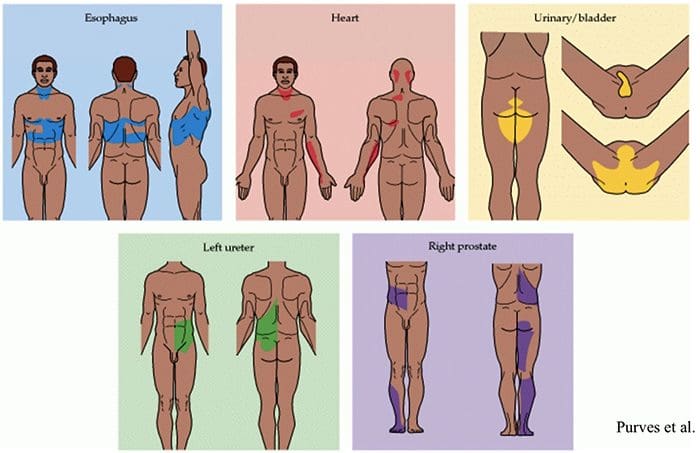
Somatovisceral refleks
Den somatoviscerale refleks er en refleks, hvor viscerale funktioner aktiveres eller hæmmes af somatisk sansestimulering. Hos forsøgsdyr har både skadelig og uskadelig stimulering af somatiske afferenter vist sig at fremkalde refleksændringer i sympatisk efferent aktivitet og følgelig effektororganfunktion. Disse fænomener er blevet vist i områder som mave-tarmkanalen, urinvejene, binyremarven, lymfeceller, hjerte og kar i hjernen og perifere nerver.
Oftest fremkaldes snit eksperimentelt ved stimulering af kutane afferenter, selvom noget arbejde også er blevet udført på muskel- og artikulære afferenter, inklusive dem af spinalceller. De ultimative svar vil repræsentere integrationen af flere toniske og reflekspåvirkninger og kan udvise lateralitet og segmentelle tendenser samt variabel excitabilitet i overensstemmelse med de involverede afferenter. I betragtning af kompleksiteten og mangfoldigheden af mekanismer involveret i det sidste udtryk for refleksresponset, bør forsøg på at ekstrapolere til kliniske situationer højst sandsynligt udføres til fordel for yderligere systematiske fysiologiske undersøgelser.
Omfanget af vores information er begrænset til kiropraktik såvel som til spinalskader og tilstande. For at diskutere emnet, er du velkommen til at spørge Dr. Jimenez eller kontakte os på 915-850-0900 .
Kurateret af Dr. Alex Jimenez
Yderligere emner: Ischias
Iskias er medicinsk omtalt som en samling af symptomer, snarere end en enkelt skade og / eller tilstand. Symptomer på sciatic nervesmerter eller ischias kan variere i hyppighed og intensitet, men det er oftest beskrevet som en pludselig, skarp (knivlignende) eller elektrisk smerte, der udstråler fra den lave ryg ned mellem balder, hofter, lår og lår benene i foden. Andre symptomer på iskias kan omfatte, prikkende eller brændende fornemmelser, følelsesløshed og svaghed langs længden af den sciatic nerve. Ischias påvirker oftest individer i alderen af 30 og 50 år. Det kan ofte udvikle sig som følge af degenerationen af rygsøjlen på grund af alder, men komprimeringen og irritationen af den sciatic nerve forårsaget af en bulging eller herniated disc, blandt andet spinal sundhed problemer, kan også forårsage sciatic nerve smerte.

EKSTRA VIGTIG TEMNE: Kiropraktor Iskias Symptomer



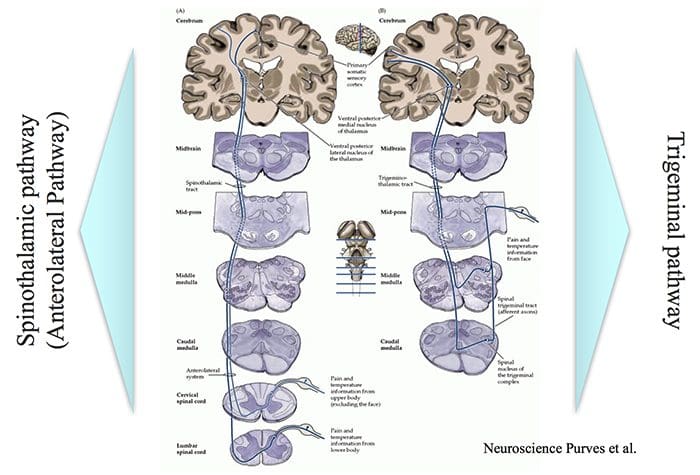
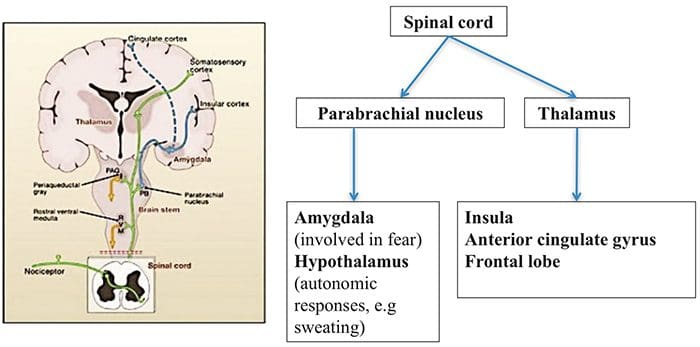 Hjerneområder involveret i behandling af nociceptive signaler
Hjerneområder involveret i behandling af nociceptive signaler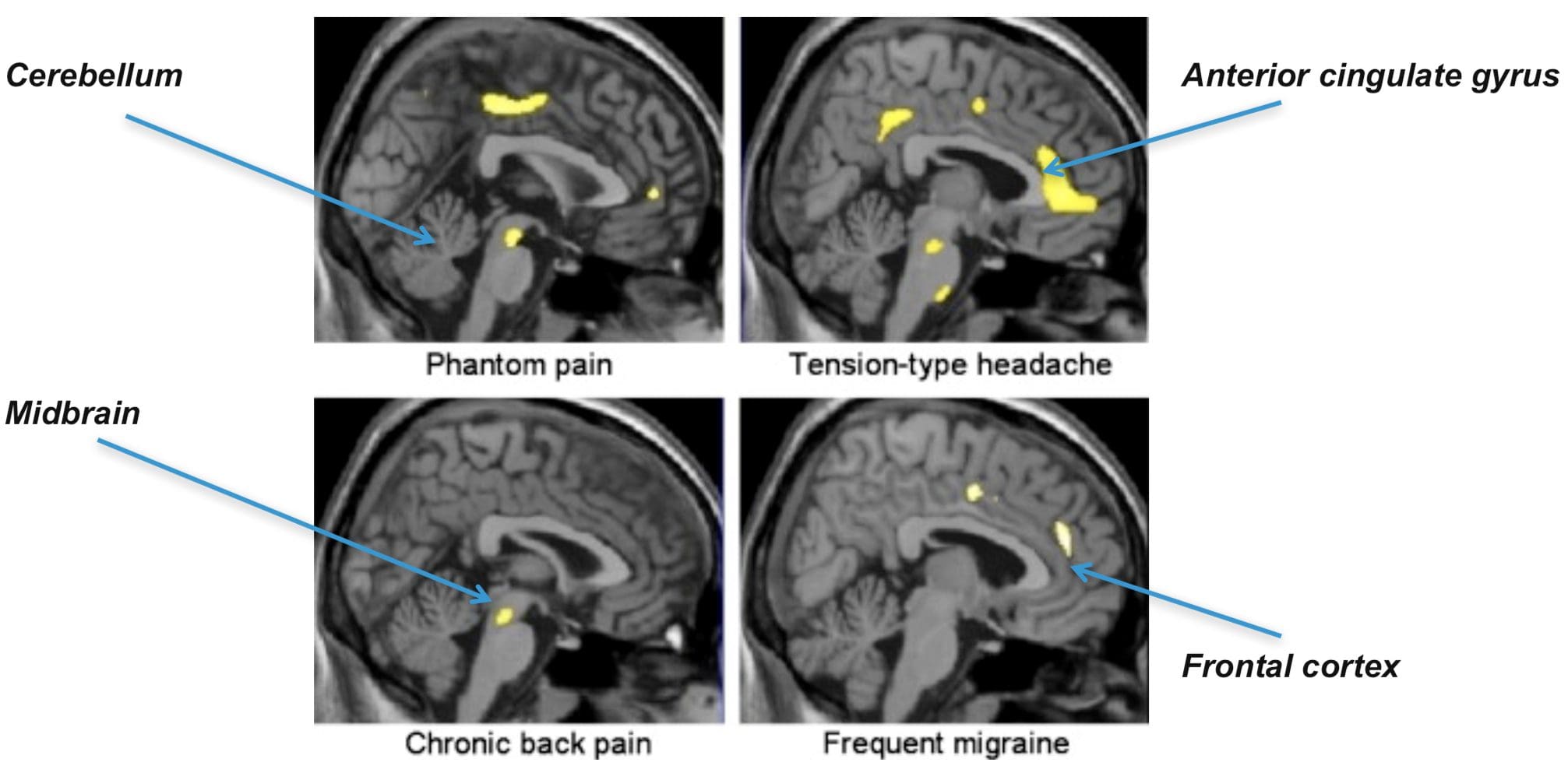 Anterior Cingulate & Insula Cortex aktiveres hos mennesker
Anterior Cingulate & Insula Cortex aktiveres hos mennesker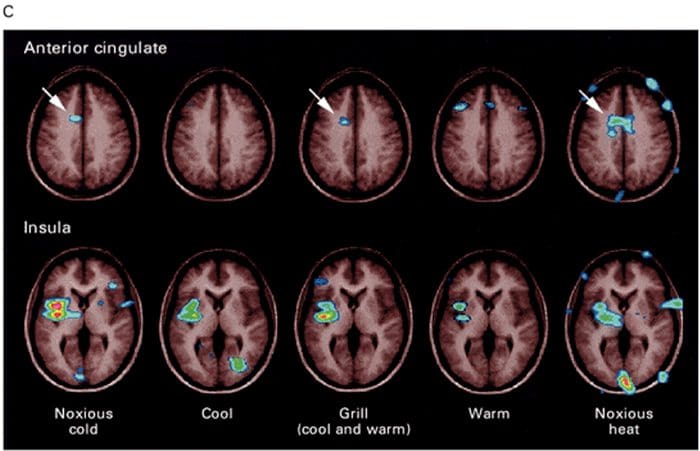
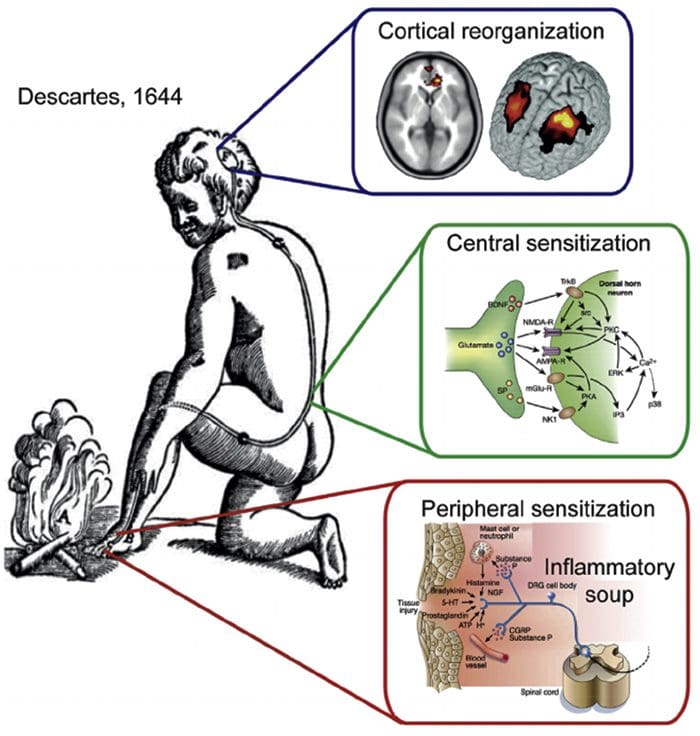
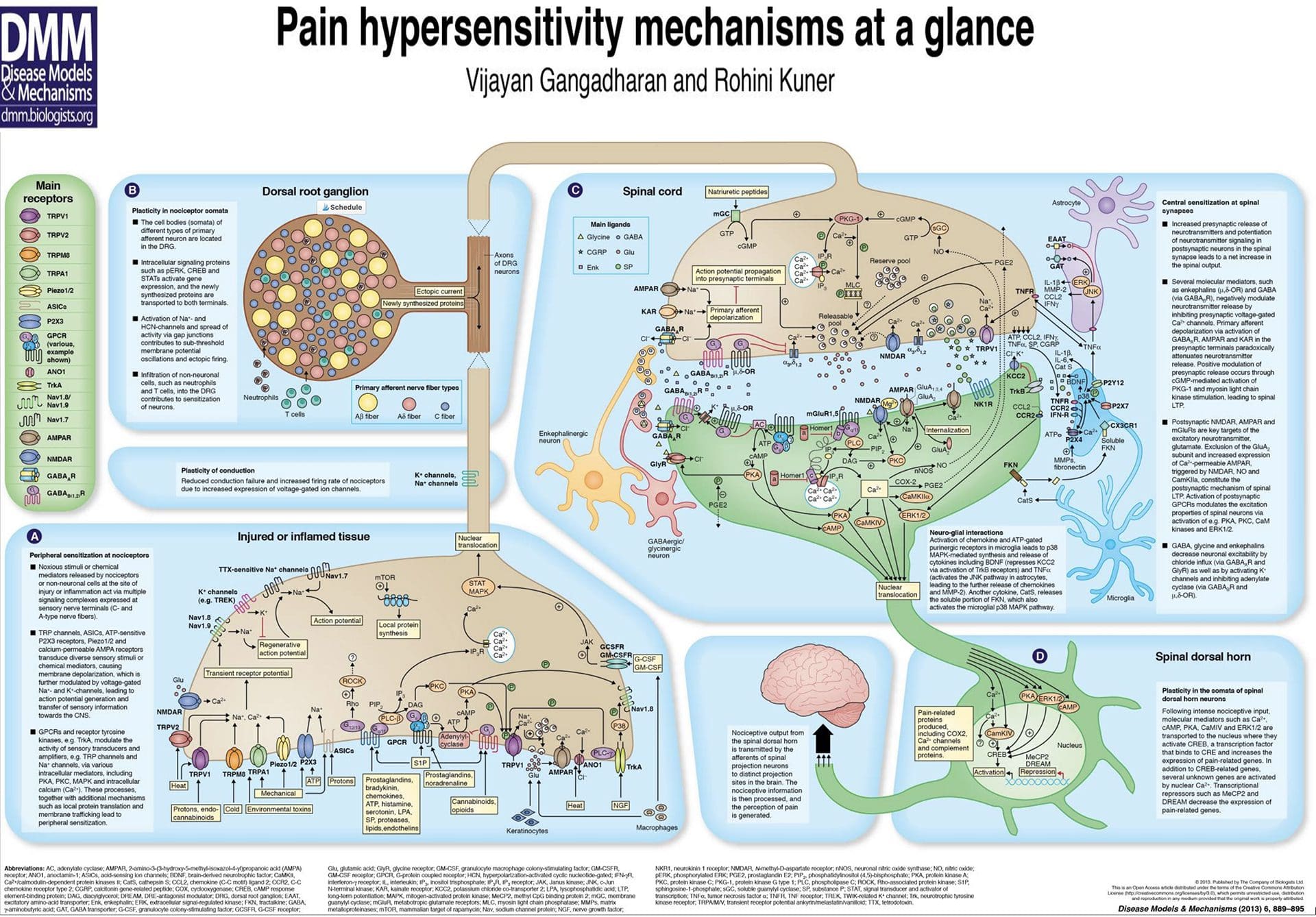
 Inflammatorisk suppe – Hyperalgesi
Inflammatorisk suppe – Hyperalgesi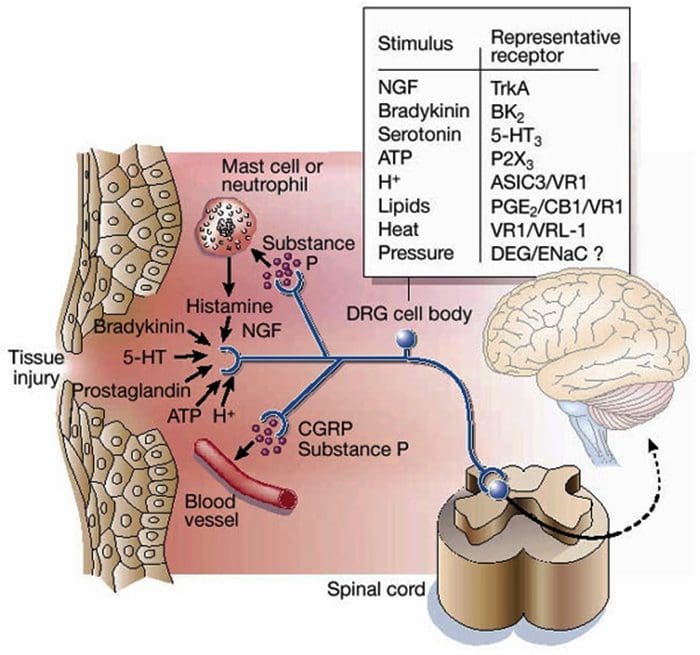
 Gate Control Theory of Pain
Gate Control Theory of Pain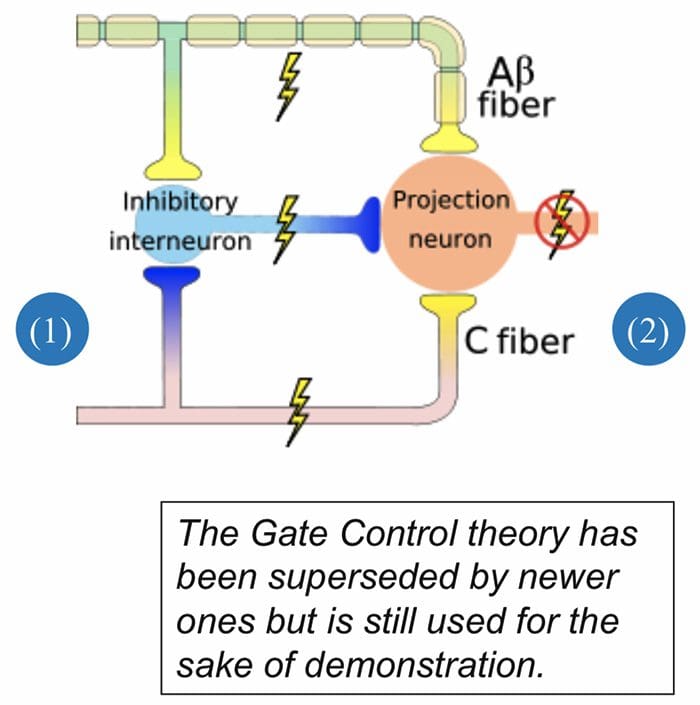
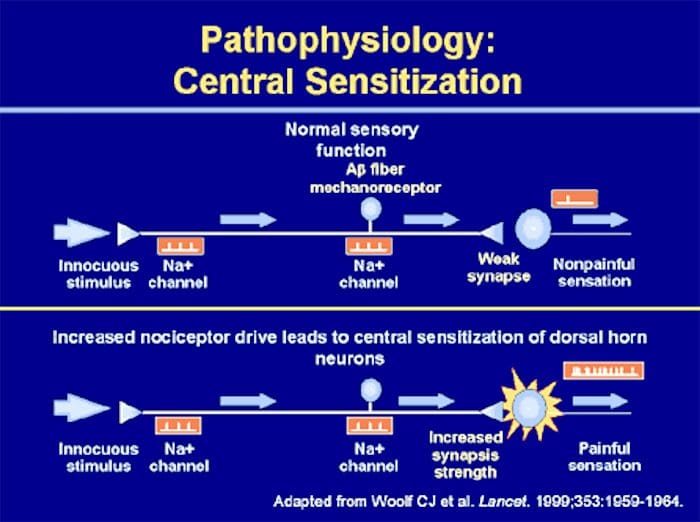
 Abnormiteter i smertesystemet
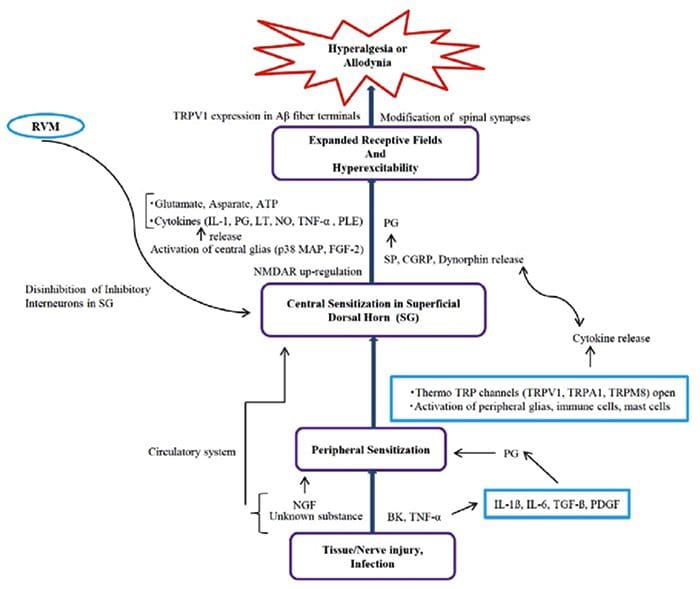
Abnormiteter i smertesystemet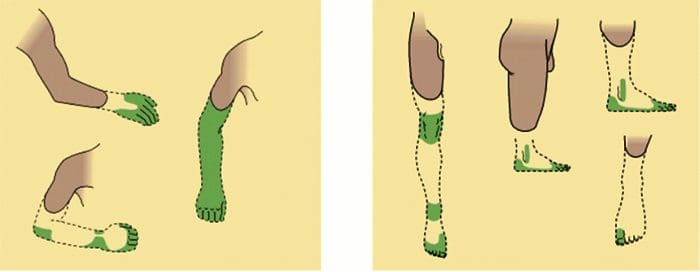 Perifer sensibilisering
Perifer sensibilisering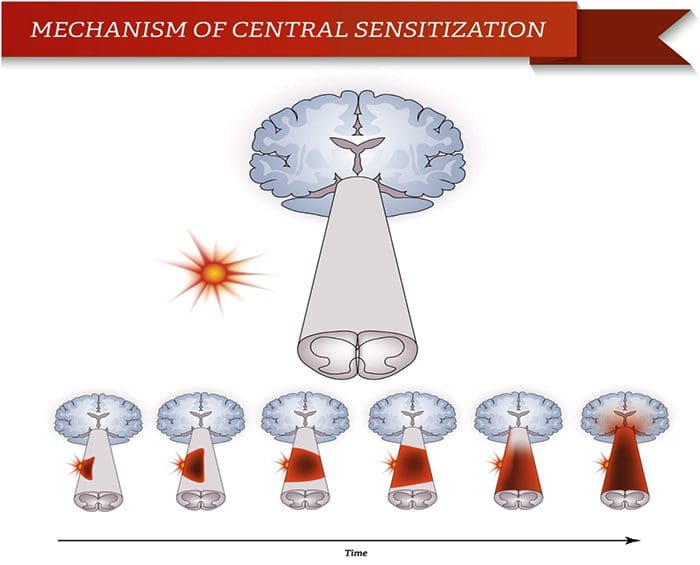
 Somatosensorisk Cortex Organisation
Somatosensorisk Cortex Organisation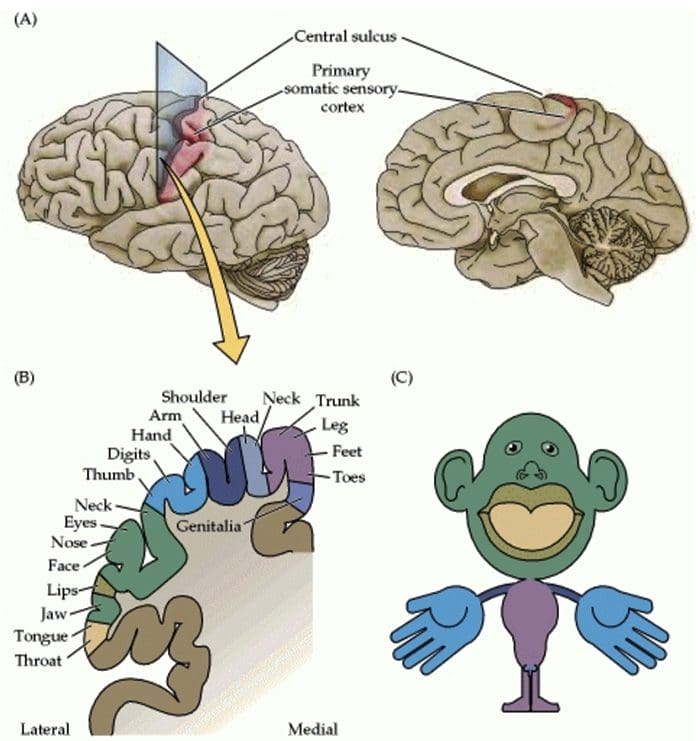 Kortikal reorganisering
Kortikal reorganisering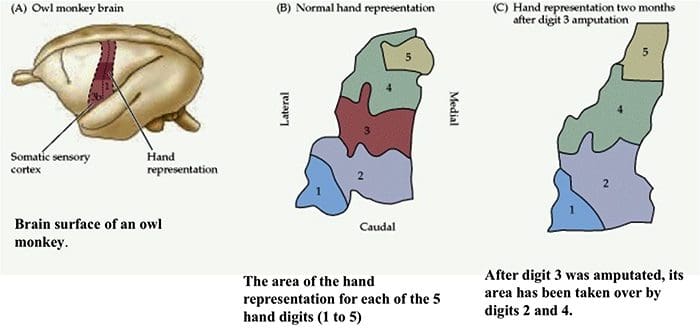

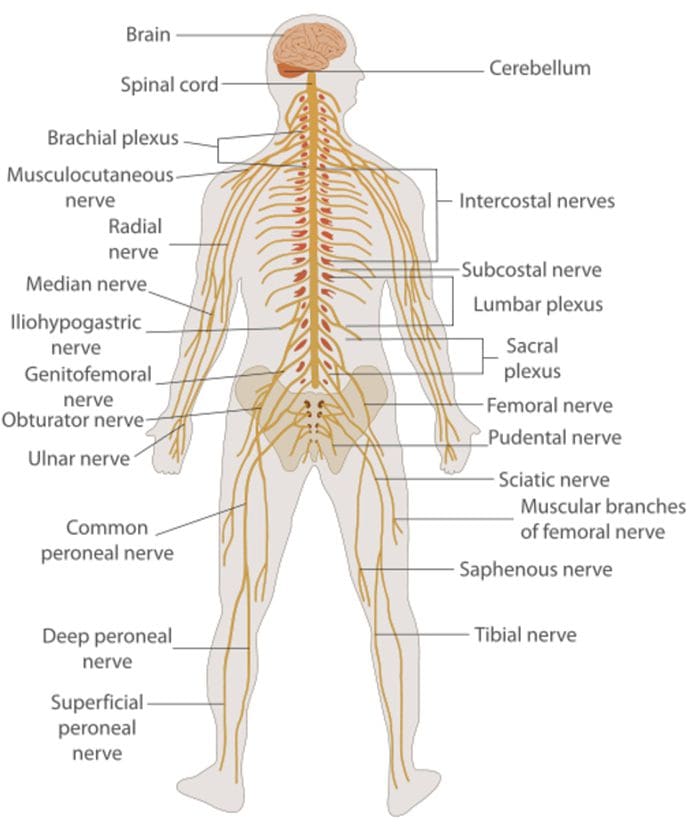
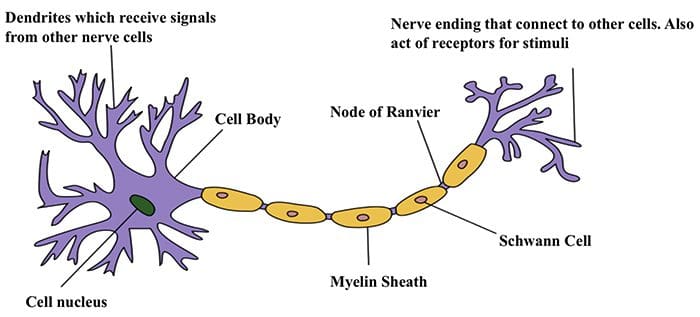 Nervecelle-til-nervecellekommunikation
Nervecelle-til-nervecellekommunikation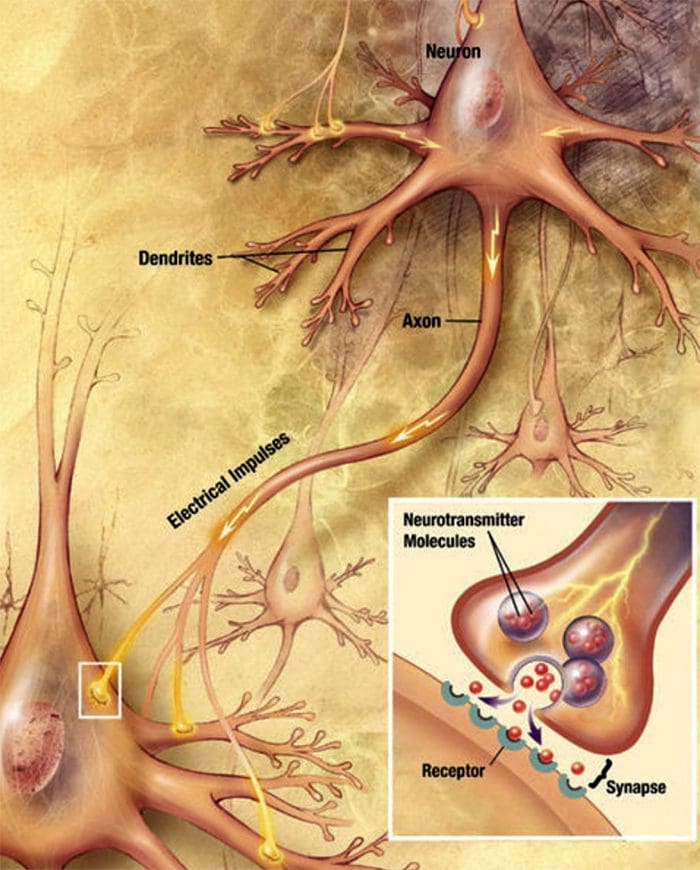 Nerveceller kommunikerer med andre celler ved at frigive et kemikalie fra nerveenderne � Neurotransmittere
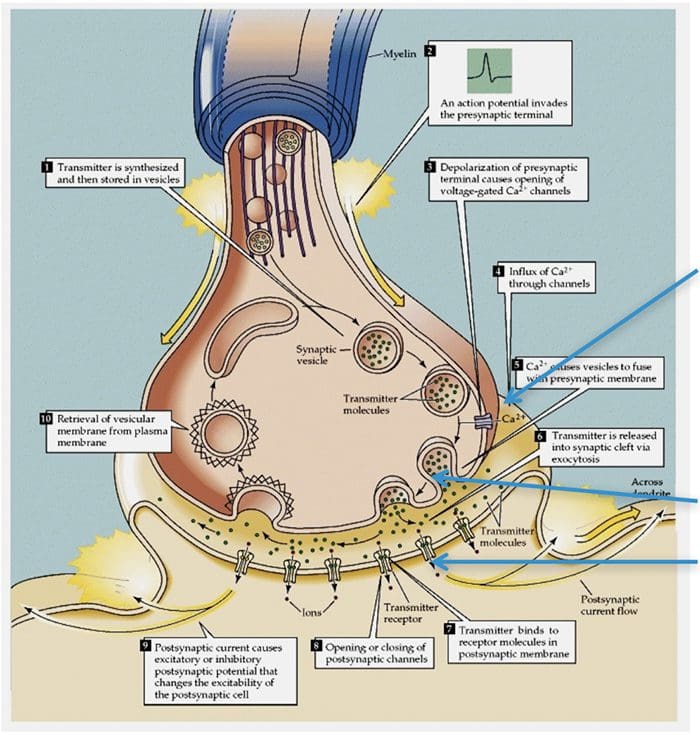
Nerveceller kommunikerer med andre celler ved at frigive et kemikalie fra nerveenderne � Neurotransmittere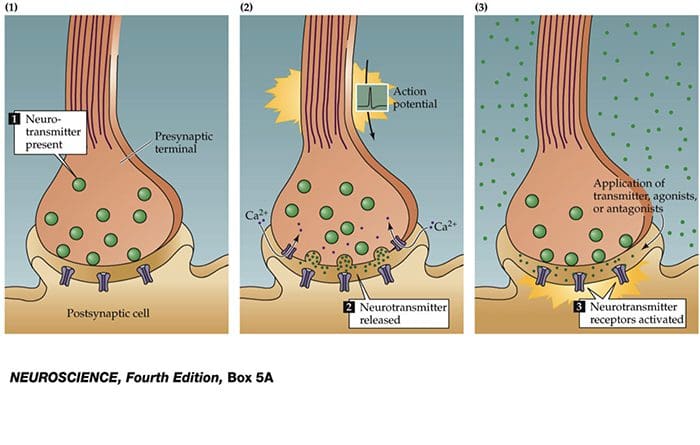
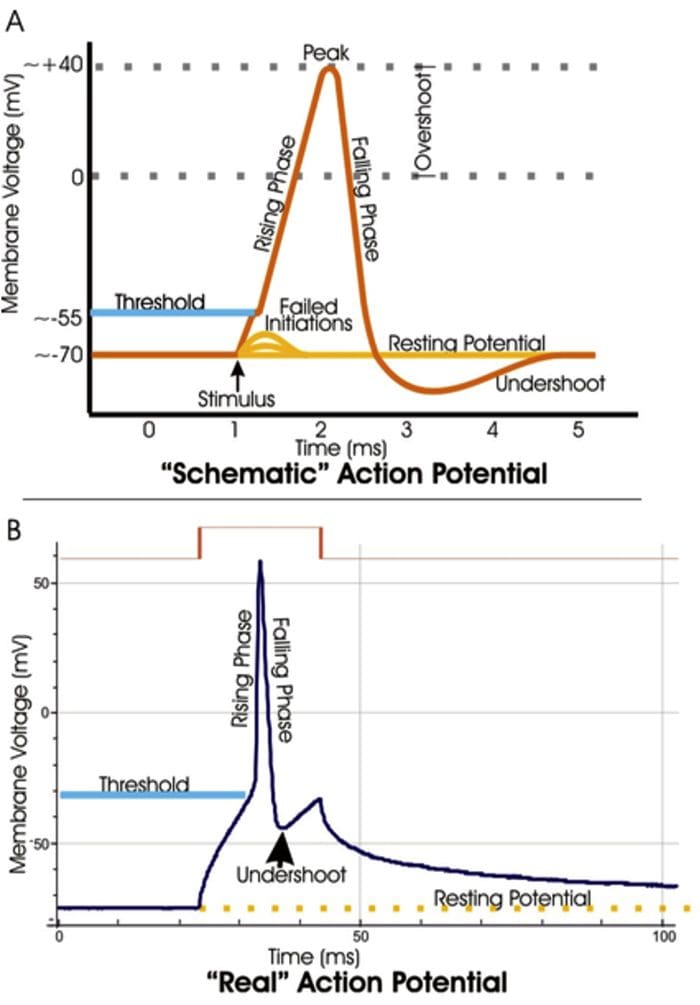
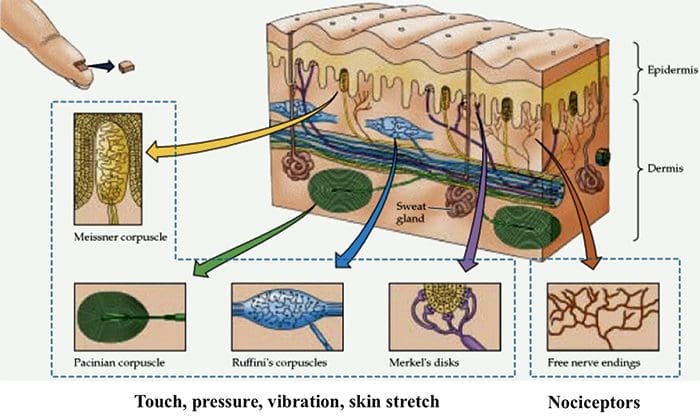
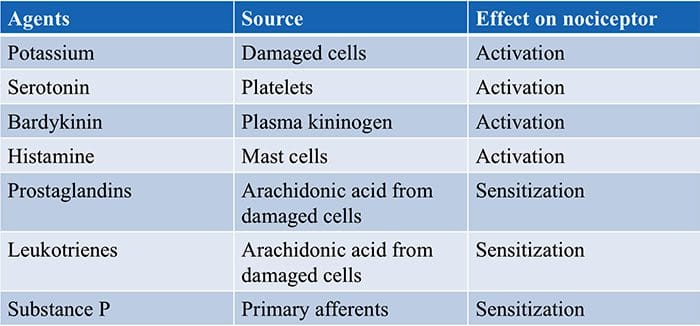
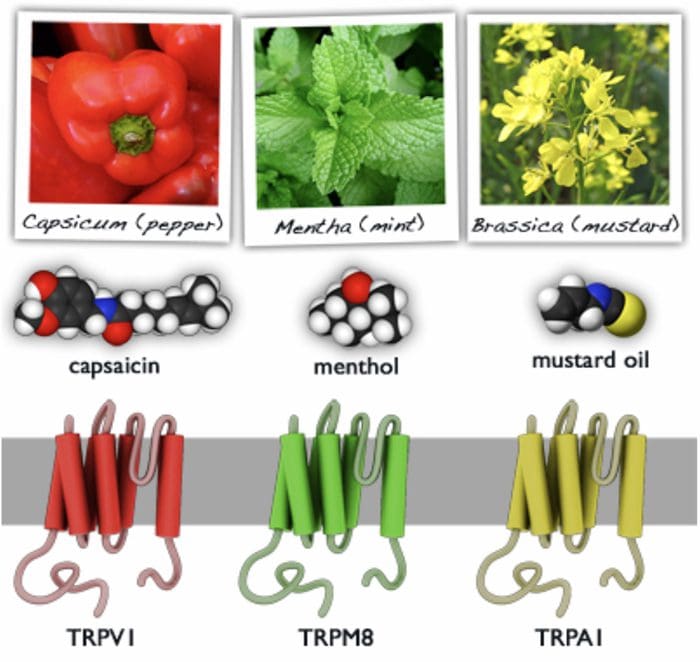
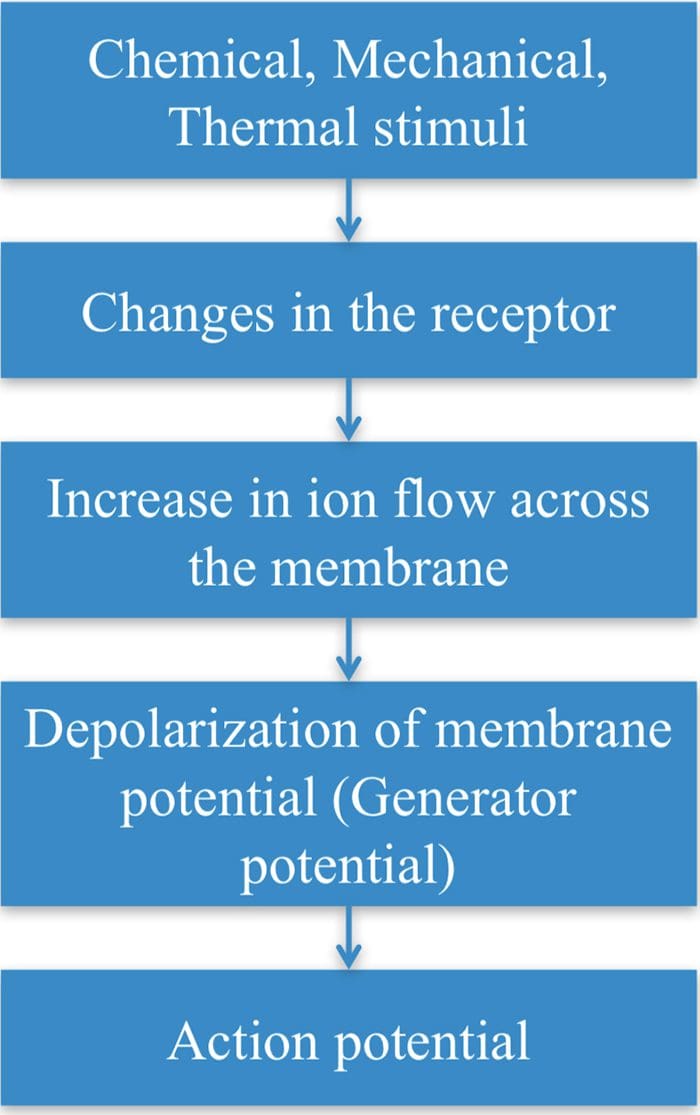 TRP kanaler
TRP kanaler