Prostatakræft: Abstrakt
Prostatacancer (PCa) er fortsat en førende årsag til dødelighed hos amerikanske mænd, og forekomsten fortsætter med at stige på verdensplan, især i lande, hvor mænd indtager en "vestlig" diæt. Epidemiologiske, prækliniske og kliniske undersøgelser tyder på en potentiel rolle for diætindtagelse på forekomsten og progressionen af PCa. 'Denne minireview giver et overblik over nyere publiceret litteratur med hensyn til næringsstoffer, kostfaktorer, kostmønstre og PCa forekomst og progression. Lavt kulhydratindtag, sojaprotein, omega-3 (w-3) fedt, grøn te, tomater og tomatprodukter og zyflamend viste løfte om at reducere PCa-risiko eller progression. Et højere indtag af mættet fedt og en højere β-carotenstatus kan øge risikoen. Der kan eksistere et U-formet forhold mellem folat, C-vitamin, D-vitamin og calcium med PCa-risiko. På trods af de inkonsekvente og uendelige resultater, er potentialet for en rolle for diætindtagelse til forebyggelse og behandling af PCa lovende. Kombinationen af alle de gavnlige faktorer for PCa-risikoreduktion i et sundt kostmønster kan være det bedste kostråd. Dette mønster inkluderer rige frugter og grøntsager, reducerede raffinerede kulhydrater, totalt og mættet fedt og reduceret kogt kød. Yderligere omhyggeligt designede prospektive forsøg er berettiget.
Nøgleord: Kost, Prostatakræft, Næringsstoffer, Kostmønster, Livsstil, Forebyggelse, Behandling, Ernæring, Diætintervention, Gennemgang
Indhold
Introduktion: Prostatakræft
Prostatacancer (PCa) er den næsthyppigste kræftsygdom hos mænd, med næsten en million nye tilfælde diagnosticeret på verdensplan om året [1], med cirka seks gange højere forekomst i vestlige lande end i ikke-vestlige lande. Kost, livsstil, miljømæssige og genetiske faktorer antages at spille en rolle i disse forskelle. Denne gennemgang fokuserer på de seneste beviser for den potentielle rolle af kostfaktorer på PCa og inkluderer epidemiologiske og kliniske forsøgsbeviser for indvirkningen af protein, fedt, kulhydrat, fibre, fytokemikalier, andre fødevarekomponenter, hele fødevarer og kostmønstre på PCa-forekomsten, udvikling og/eller progression. Data fra metaanalyser eller veldesignede randomiserede forsøg og prospektive undersøgelser fremhæves i denne gennemgang. Det skal bemærkes, at undersøgelser af kostindtag eller ernæring og kræft ofte er underlagt forskellige begrænsninger og dermed vanskeliggør tolkning af resultater. For eksempel, når en undersøgelse er designet til at undersøge effekten af mængden af fedtindtag, vil ændring i fedtindtaget uundgåeligt ændre indtaget af protein og/eller kulhydrat og kan også ændre indtaget af andre næringsstoffer. Som følge heraf er det svært at tilskrive effekten alene til ændring i fedtindtaget. Derudover involverer virkningen af makronæringsstoffer potentielt aspekter af både absolut mængde og typen af forbrugte makronæringsstoffer. Begge aspekter kan potentielt påvirke kræftinitiering og/eller udvikling uafhængigt, men de kan ikke altid skelnes i forskningsdesign. Selvom dette emne for nylig blev gennemgået [2], i betragtning af den omfattende nye litteratur om emnet, præsenteres en opdateret gennemgang heri, og en sammenfattende tabel er tilvejebragt for en hurtig reference (tabel 1).
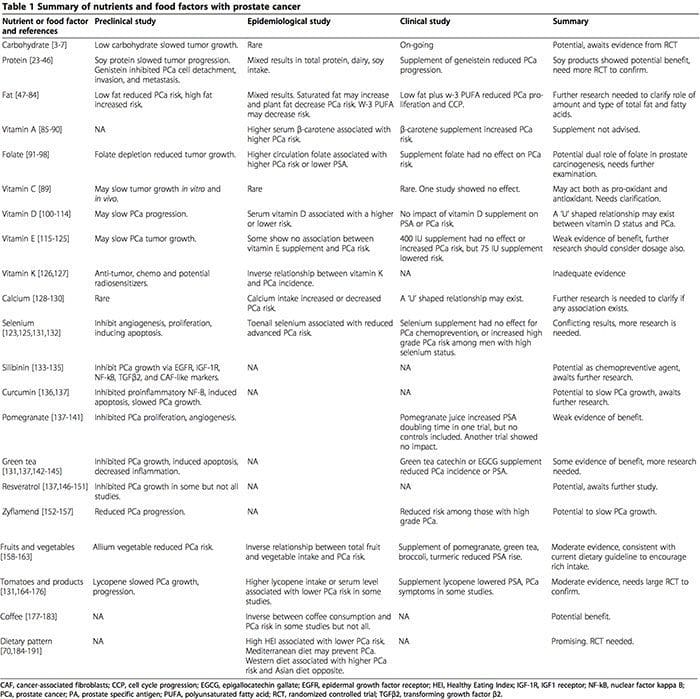
Næringsstoffer Kulhydrater Givet hypotesen om, at insulin er en vækstfaktor for PCa, er det blevet antaget, at reduktion af kulhydrater og dermed sænkning af seruminsulin kan bremse PCa-væksten [3]. I dyremodeller har enten en ketogen diæt uden kulhydrat (NCKD) [4,5] eller en diæt med lavt kulhydratindhold (20 % kcal som kulhydrat) gunstige effekter på at bremse prostatatumorvækst [6,7]. I humane undersøgelser fandt en undersøgelse, at højt indtag af raffinerede kulhydrater var forbundet med øget risiko for PCa [7]. Ud over mængden af kulhydrater kan typen af kulhydrater påvirke PCa, men forskningen har ikke været entydig. Potentialet for at reducere PCa-risikoen og progression ved at påvirke kulhydratmetabolismen undersøges aktivt med Metformin. Metformin reducerede PCa-celleproliferation og forsinket progression in vitro og in vivo henholdsvis [8-10] og reducerede hændelsesrisiko og dødelighed hos mennesker [11-13]. To enkeltarmede kliniske forsøg viste også en positiv effekt af metformin til at påvirke markører for PCa-proliferation og progression [14,15]. Andre retrospektive kohortestudier har dog ikke understøttet en effekt af metformin på tilbagefald eller hændelsesrisiko for PCa [16-22]. På trods af potentialet for at reducere enten totale eller simple kulhydrater til gavn for PCa-kontrol, mangler beviser fra randomiserede kontrollerede forsøg (RCT). To randomiserede undersøgelser er i gang, hvor man undersøger virkningen af en diæt med lavt kulhydrat (ca. 5 % kcal) på PSA-fordoblingstiden blandt PCa-patienter efter radikal prostatektomi (NCT01763944) og på glykæmisk respons blandt patienter, der starter behandling med androgendeprivation (ADT) ( NCT00932672). Resultater fra disse forsøg vil kaste lys over effekten af kulhydratindtag på markører for PCa-progression og den rolle, reduceret kulhydratindtag spiller for at udligne bivirkningerne af ADT.
Protein
Det ideelle niveau af proteinindtag for optimal generel sundhed eller prostata sundhed er uklart. På trods af populariteten af diæter med lavt kulhydratindhold, der er højt i protein, rapporterede nyere menneskelige undersøgelser, at lavt proteinindtag var forbundet med lavere risiko for kræft og generel dødelighed blandt mænd 65 og yngre. Blandt mænd over 65 år var lavt proteinindtag forbundet med en højere risiko for kræft og overordnet dødelighed [23]. I dyremodeller påvirkede forholdet mellem protein og kulhydrat på kardiometabolisk sundhed, aldring og levetid [24]. Rollen af kostprotein og protein til kulhydrat-forholdet på PCa udvikling og progression kræver yderligere undersøgelse.
Dyrebaserede proteiner
At studere proteinindtag, som alle aspekter af ernæringsvidenskab, kan være udfordrende. For eksempel består animalsk kød, som er en proteinkilde i vestlige kostvaner, ikke kun af protein, men også af fedt, kolesterol, mineraler og andre næringsstoffer. Mængden af disse næringsstoffer inklusive fedtsyrer kan variere fra det ene dyrekød til det andet. Tidligere undersøgelser på mennesker har vist, at indtagelse af hudløst fjerkræ, som er lavere i kolesterol og mættet fedt end mange røde kød, ikke var forbundet med tilbagefald eller progression af PCa [25]. Indtagelse af bagt fjerkræ var imidlertid omvendt forbundet med avanceret PCa [26,27], mens kogt rødt kød var forbundet med øget avanceret PCa-risiko [26,27]. Hvordan maden tilberedes kan således ændre dens indvirkning på PCa-risiko og progression. Samlet set kan fiskeforbrug være forbundet med reduceret PCa-dødelighed, men kogt fisk ved høj temperatur kan bidrage til PCa-karcinogenese [28]. Det kan derfor være tilrådeligt at indtage fisk regelmæssigt, men tilberedningstemperaturen bør holdes moderat.
Mejeribaseret protein
En anden almindelig proteinkilde er mejeriprodukter, såsom mælk, ost og yoghurt. Tidligere undersøgelser har vist, at mejeriprodukter øgede den samlede PCa-risiko, men ikke med aggressiv eller dødelig PCa [29,30]. Derudover blev både sødmælk og mælkeforbrug med lavt fedtindhold rapporteret at enten fremme eller forsinke PCa-progression [29,31]. I Physicians Health opfølgningskohorten med 21,660 mænd blev det samlede mejeriforbrug fundet at være forbundet med øget PCa-incidens [32]. Især øgede fedtfattig eller skummetmælk lavkvalitets PCa, mens sødmælk øgede dødelig PCa-risiko. Selvom den/de nøjagtige komponent(er) af mejeriprodukter, der driver disse associationer, er ukendt, kan de høje koncentrationer af mættet fedt og calcium være involveret. En tværsnitsundersøgelse af 1798 mænd viste, at mejeriprotein var positivt forbundet med serum IGF-1 [33] niveauer, hvilket kan stimulere initiering eller progression af PCa. Der er således behov for yderligere forskning for at klarlægge sammenhængen mellem mælkeindtag og PCa. Der er utilstrækkelige data til at give anbefalinger specifikt relateret til mejeri- eller mejeriprotein og PCa-risiko eller progression.
Plantebaserede proteiner
Soja og sojabaserede produkter er rige på protein og phytoøstrogener, der kan lette PCa-forebyggelse, men dens rolle på PCa er uklar. I en undersøgelse med mus var indtagelse af sojaprodukter forbundet med nedsat leveraromatase, 5?-reduktase, ekspression af androgenreceptor og dens regulerede gener, FOXA1, urogenital kanalvægt og PCa-tumorprogression [34]. Et nyligt randomiseret forsøg med 177 mænd med højrisikosygdomme efter radikal prostatektomi fandt, at sojaproteintilskud i to år ikke havde nogen effekt på risikoen for PCa-gentagelse [35]. Selvom epidemiologiske og prækliniske undersøgelser [36,37] understøtter en potentiel rolle for soja/sojaisoflavoner i PCa risikoreduktion eller progression, fandt en meta-analyse ikke signifikant effekt af sojaindtag i PSA-niveauer, kønshormonbindende globulin, testosteron, fri testosteron, østradiol eller dihydrotestosteron [38]. En anden RCT hos patienter før prostatektomi fandt heller ikke nogen effekt af sojaisoflavontilskud op til seks uger på PSA, serum totalt testosteron, frit testosteron, total østrogen, østradiol eller total kolesterol [39]. Da de fleste RCT'er, der er udført, har været små og af kort varighed, er yderligere undersøgelse nødvendig.
Mange undersøgelser har fortsat med at undersøge den primære isoflavon i soja, genistein og dens effekt på PCa. Potentialet for genistein til at hæmme PCa-celleløsning, invasion og metastaser er rapporteret [40]. Genistein kan modificere glukoseopdatering og glukosetransportør (GLUT) ekspression i PCa-celler [41] eller udøve sin antitumoreffekt ved at nedregulere flere mikroRNA'er [42]. Undersøgelser, der anvender tumorceller og dyremodeller, tyder på, at genistein kan konkurrere med og blokere endogene østrogener fra at binde sig til østrogenreceptoren og derved hæmme cellulær proliferation, vækst og inducere differentiering, og specifikt kan genistein hæmme celleløsning, proteaseproduktion, celleinvasion og dermed forebygge metastaser [36,40,43]. Imidlertid var hverken plasma- eller urinniveauer af genistein forbundet med PCa-risiko i case-kontrolstudier [44,45]. I en fase 2 placebo-kontrolleret RCT med 47 mænd reducerede tilskud af 30 mg genistein i tre til seks uger signifikant androgen-relaterede markører for PCa-progression [46]. Derudover kan genistein være gavnligt til at forbedre cabazitaxel kemoterapi i metastatisk kastrationsresistent PCa [37]. Kliniske undersøgelser er berettiget til yderligere at undersøge soja- og sojaisoflavonernes rolle til forebyggelse eller behandling af PCa. En endelig anbefaling vedrørende proteinindtag til PCa-forebyggelse eller behandling er ikke tilgængelig endnu.
Fedt
Forskningsresultater, der undersøger fedtforbrug med PCa-risiko eller progression, er modstridende. Både det totale absolutte indtag [47] af fedt fra kosten og den relative fedtsyresammensætning kan uafhængigt relatere til PCa-initiering og/eller progression. Mens dyreforsøg gentagne gange viser, at reduktion af kostens fedtindtag sænker tumorvækst [48-50] og kost med højt fedtindhold, især animalsk fedt og majsolie øger PCa-progressionen [51], er menneskelige data mindre konsistente. Casekontrolstudier og kohortestudier har vist enten ingen sammenhæng mellem totalt fedtforbrug og PCa-risiko [52-55] eller en omvendt sammenhæng mellem fedtindtag og PCa-overlevelse, især blandt mænd med lokaliseret PCa [47]. Derudover viste et tværsnitsstudie, at fedtindtag udtrykt som procent af det samlede kalorieindtag var positivt forbundet med PSA-niveauer hos 13,594 mænd uden PCa [56]. I betragtning af disse modstridende data er det muligt, at typen af fedtsyre [56] snarere end den samlede mængde kan spille en vigtig rolle i PCa udvikling og progression. En undersøgelse fandt, at plasmamættede fedtsyrer var positivt forbundet med PCa-risiko i en prospektiv kohorte på 14,514 mænd fra Melbourne Collaborative Cohort Study [57]. Derudover fandt en anden undersøgelse, at at spise mere plantebaseret fedt var forbundet med reduceret PCa-risiko [58]. Disse undersøgelser understøtter den nuværende kostvejledning om at spise mindre animalsk fedt og mere plantebaseret fedt.
Data vedrørende forbrug af omega-6 (w-6) og omega-3 (w-3) flerumættede fedtsyrer (PUFA) og PCa-risiko er også modstridende. Selvom der er data, der understøtter en sammenhæng mellem øget w-6 PUFA-indtag (hovedsageligt afledt af majsolie) og risikoen for samlet og højkvalitets PCa [57,59], understøtter ikke alle data et sådant link [60]. Faktisk var et større indtag af flerumættet fedt forbundet med en lavere dødsfald blandt mænd med ikke-metastatisk PCa i Health Professionals Follow-up-undersøgelsen [58]. Den postulerede mekanisme, der forbinder w-6 PUFA'er og PCa-risiko er omdannelsen af arachidonsyre (w-6 PUFA) til eicosanoider (prostaglandin E-2, hydroxyeicosatetraensyrer og epoxyeicosatriensyrer), der fører til inflammation og cellulær vækst [61]. Omvendt kan w-3 PUFA'er, som primært findes i koldtvandsfedte fisk, bremse væksten af PCa gennem en række mekanismer [61-63]. I en undersøgelse af 48 mænd med lav risiko PCa under aktiv overvågning viste gentagen biopsi i seks måneder, at prostatavævets w-3 fedtsyrer, især eicosapentaensyre (EPA), kan beskytte mod PCa progression [64]. In vitro og dyreforsøg tyder på, at w-3 PUFA'er inducerer antiinflammatoriske, pro-apoptotiske, antiproliferative og anti-angiogene veje [65,66]. Desuden viste en museundersøgelse, der sammenlignede forskellige typer fedt, at kun fiskeoliediæten (det vil sige omega-3-baseret kost) bremsede PCa-væksten i forhold til andre diætfedtstoffer [67]. Med hensyn til humane data viste et fase II randomiseret forsøg, at en fedtfattig diæt med w-3-tilskud fire til seks uger før radikal prostatektomi reducerede PCa-proliferation og cellecyklusprogression (CCP) score [62,68]. En fedtfattig fiskeoliediæt resulterede i nedsatte 15(S)-hydroxyeicosatetraensyreniveauer og sænket CCP-score i forhold til en vestlig kost [69]. De potentielle fordele ved omega-3-fedtsyrer fra fisk understøttes af epidemiologisk litteratur, der viser, at w-3-fedtsyreindtag var omvendt forbundet med dødelig PCa-risiko [70,71]. På trods af løftet om omega-3 fedtsyrer er ikke alle undersøgelser enige. Supplering af 2 g alfa-linolensyre (ALA) om dagen i 40 måneder hos 1,622 mænd med PSA <4 ng/ml ændrede ikke deres PSA [72]. En anden undersøgelse fandt imidlertid, at et højt blodserum n-3 PUFA og docosapentaensyre (DPA) var forbundet med reduceret total PCa-risiko, mens høj serum-EPA og docosahexaensyre (DHA) muligvis var forbundet med øget højgradig PCa-risiko [73] . Yderligere forskning er påkrævet for bedre at forstå rollen af omega-3 PUFA'er i PCa-forebyggelse eller -behandling.
Kolesterol
Mange prækliniske undersøgelser har vist, at akkumulering af kolesterol bidrager til progressionen af PCa [74-76]. Det blev foreslået, at et højt kolesteroltal i Lin et al. BMC Medicine (2015) 13:3 Side 5 af 15 cirkulation kan være en risikofaktor for solide tumorer, primært gennem opregulering af kolesterolsyntese, inflammatoriske veje [77] og intratumoral steroidogenese [78]. Ifølge en nylig undersøgelse med 2,408 mænd planlagt til biopsi, var serumkolesterol uafhængigt forbundet med forudsigelse af PCa-risiko [79]. I overensstemmelse med kolesterolfundene var brugen af det kolesterolsænkende lægemiddel statin efter radikal prostatektomi (RP) signifikant forbundet med reduceret risiko for biokemisk tilbagefald hos 1,146 patienter med radikal prostatektomi [80]. En anden undersøgelse viste også, at statiner kan reducere PCa-risikoen ved at sænke progression [81]. Selvom mekanismen ikke er blevet etableret, viste nyere undersøgelser også, at et lavt high-density lipoprotein (HDL) kolesterolniveau var forbundet med en højere risiko for PCa, og derfor var et højere HDL beskyttende [81-84]. Disse resultater understøtter forestillingen om, at en hjertesund diætintervention, der sænker kolesterol, også kan gavne prostatasundheden.
Vitaminer & mineraler
Heri vil vi gennemgå de seneste data om vitamin A, B-kompleks, C, D, E og K og selen. I de to store kliniske forsøg: Carotene and Retinol Efficacy Trial (CARET; PCa var et sekundært resultat) og National Institutes of Health-American Association of Retired Persons (NIH-AARP) kost- og sundhedsprospektive kohorteundersøgelse, var overdreven multivitamintilskud forbundet med en højere risiko for at udvikle aggressiv PCa, især blandt dem, der tager individuelle β-carotentilskud [85,86]. På samme måde var høje serum-β-carotenniveauer forbundet med en højere risiko for PCa blandt 997 finske mænd i Kuopio Iskæmisk hjertesygdomsrisikofaktor-kohorte [87]. Imidlertid blev ?-carotentilskud ikke fundet at påvirke risikoen for dødelig PCa under behandling [88] eller i det danske prospektive kohortestudie af 26,856 mænd [89]. Cirkulerende retinol var heller ikke forbundet med PCa-risiko i et stort case-kontrolstudie [90]. Derfor er sammenhængen mellem vitamin A og PCa stadig uklar.
Prækliniske beviser tyder på, at folatudtømning kan bremse tumorvækst, mens tilskud ikke har nogen effekt på vækst eller progression, men kan direkte føre til epigenetiske ændringer via stigninger i DNA-methylering [91]. To metaanalyser viste også, at cirkulerende folatniveauer var positivt forbundet med en øget risiko for PCa [92,93], mens diæt eller supplerende folat ikke havde nogen effekt på PCa-risikoen [94] i et kohortestudie med 58,279 mænd i Holland [95] 96] og en case-kontrolundersøgelse i Italien og Schweiz [97]. Faktisk viste en undersøgelse af en kohorte af mænd, der gennemgår radikal prostatektomi på flere Veterans Administration-faciliteter i hele USA, endda, at højere serumfolatniveauer var forbundet med lavere PSA og dermed lavere risiko for biokemisk svigt [2007]. En anden undersøgelse, der bruger data fra 2010 til XNUMX National Health and Ernæring Undersøgelsesundersøgelse viste, at en højere folatstatus kan være beskyttende mod forhøjede PSA-niveauer blandt 3,293 mænd, 40 år og ældre, uden diagnosticeret PCa [98]. Det blev foreslået, at folat kan spille en dobbelt rolle i prostatacarcinogenese, og derfor afventer det komplekse forhold mellem folat og PCa yderligere undersøgelse [99].
På trods af C-vitamins (ascorbinsyre) potentielle rolle som en antioxidant i kræftbehandling, er forsøg, der undersøger kostindtag eller tilskud af C-vitamin, få. En RCT viste ingen effekt af C-vitaminindtag på PCa-risiko [89]. Desuden kan C-vitamin i høje doser fungere mere som en pro-oxidant end antioxidant, hvilket komplicerer forskningsdesignet og fortolkningen.
Den primære aktive form af vitamin D, 1,25 dihydroxyvitamin D3 (calcitriol) hjælper med korrekt knogledannelse, inducerer differentiering af nogle immunceller og hæmmer protumorveje, såsom proliferation og angiogenese, og er blevet foreslået at gavne PCa-risikoen [100]; resultaterne er dog fortsat usikre. Nyere undersøgelser viste, at øgede serum-vitamin D-niveauer var forbundet med nedsat PCa-risiko [101,102]. Yderligere kan tilskud af D-vitamin bremse PCa-progression eller inducere apoptose i PCa-celler [103-105]. Andre undersøgelser rapporterede imidlertid enten ingen indvirkning af vitamin D-tilskud på PSA [106] eller ingen effekt af vitamin D-status på PCa-risiko [107,108]. Nogle undersøgelser rapporterede modsat, at en lavere D-vitaminstatus var forbundet med en lavere PCa-risiko hos ældre mænd [109], eller et højere serum D-vitamin var forbundet med en højere PCa-risiko [110,111]. En undersøgelse antydede endda, at der kan eksistere et U-formet forhold mellem D-vitaminstatus og PCa, og det optimale udvalg af cirkulerende D-vitamin til PCa-forebyggelse kan være snævert [112]. Dette stemmer overens med resultaterne for andre næringsstoffer om, at et større indtag af et gunstigt næringsstof ikke altid er bedre.
En nylig undersøgelse viste, at sammenhængen mellem D-vitamin og PCa blev moduleret af D-vitamin-bindende protein [113], hvilket kan have delvist forklaret de tidligere inkonsekvente fund. Yderligere rapporterede en meta-analyse, der undersøgte sammenhængen mellem vitamin D-receptor (VDR) polymorfismer (BsmI og FokI) og PCa-risiko, ingen sammenhæng med PCa-risiko [114]. Derfor er D-vitamins rolle i PCa stadig uklar.
I et stort randomiseret forsøg med i alt 14,641 amerikanske mandlige læger på 50 år, modtog deltagerne tilfældigt 400 IE vitamin E hver anden dag i et samlet gennemsnit på 10.3 (13.8) år. E-vitamintilskud havde ingen umiddelbare eller langsigtede virkninger på risikoen for total cancer eller PCa [115]. Imidlertid resulterede en moderat dosis af vitamin E-tilskud (50 mg eller omkring 75 IE) i lavere PCa-risiko blandt 29,133 finske mandlige rygere [116]. Flere prækliniske undersøgelser tyder på, at E-vitamin bremser tumorvækst, delvist på grund af hæmning af DNA-syntese og inducering af apoptotiske veje [117]. Desværre har undersøgelser på mennesker været mindre end støttende. To observationsstudier (Cancer Prevention Study II Nutrition Cohort og NIH-AARP Diet and Health Study) viste begge ingen sammenhæng mellem vitamin E-tilskud og PCa-risiko [118,119]. Imidlertid var et højere serum β-tocopherol, men ikke β-tocopherol niveauet forbundet med nedsat risiko for PCa [120,121], og associationen kan modificeres af genetiske variationer i vitamin E relaterede gener [122]. Tværtimod viste et prospektivt randomiseret forsøg, Selenium and Vitamin E Cancer Prevention Trial (SELECT), vitamin E-tilskud signifikant øget PCa-risiko [123], og at et højere plasma-β-tocopherol niveau kan interagere med selentilskud for at øge høj kvalitet PCa-risiko [124]. Dette fund er i overensstemmelse med et case-kohortestudie af 1,739 tilfælde og 3,117 kontroller, der viste E-vitamin øget PCa-risiko blandt dem med lav selenstatus, men ikke dem med høj selenstatus [125]. Der er således behov for mere forskning for at undersøge sammenhængen mellem E-vitamin og PCa, og dosiseffekten og interaktionen med andre næringsstoffer bør overvejes.
Vitamin K er blevet antaget til at hjælpe med at forhindre PCa ved at reducere biotilgængeligt calcium. Prækliniske undersøgelser viser, at kombinationen af vitamin C og K har potent antitumoraktivitet in vitro og virker som kemo- og radiosensibilisatorer in vivo [126]. Til dato har få undersøgelser undersøgt dette, selvom en undersøgelse, der brugte European Prospective Investigation into Cancer and Nutrition (EPIC)-Heidelberg-kohorte, fandt et omvendt forhold mellem vitamin K (som menaquinoner) indtag og PCa-forekomst [127]. Lidt eller ingen prækliniske undersøgelser er blevet udført for at undersøge calciums rolle med PCa. Retrospektive og metaanalyser tyder på øget eller reduceret PCa-risiko med øget calciumindtag, mens andre tyder på ingen sammenhæng [128,129]. En anden undersøgelse tyder på en �U�-formet association, hvor meget lave calciumniveauer eller tilskud begge er forbundet med PCa [130].
Selen er på den anden side blevet antaget for at forhindre PCa. Mens in vitro undersøgelser antydede, at selen hæmmede angiogenese og proliferation, mens det inducerede apoptose [131], viste resultater fra SELECT ingen fordele ved selen alene eller i kombination med vitamin E til PCa kemoforebyggelse [123]. Desuden gavnede selentilskud ikke mænd med lav selenstatus, men øgede risikoen for højgradig PCa blandt mænd med høj selenstatus i en tilfældigt udvalgt kohorte på 1,739 tilfælde med højgradig (Gleason 7�10) PCa og 3,117 kontroller [ 125]. Et prospektivt hollandsk kohortestudie, som omfattede 58,279 mænd, 55- til 69-årige, viste også, at tånegleselen var forbundet med en reduceret risiko for fremskreden PCa [132]. Yderligere forskning er nødvendig for at afklare selens rolle med PCa.
fytokemikalier
Sammen med vitaminer og mineraler [2] indeholder planter fytokemikalier med potentielle anti-kræfteffekter. Typisk ikke betragtes som essentielle forbindelser, fytokemikalier har antioxidant og anti-inflammatoriske egenskaber.
Silibinin er et polyfenolisk flavonoid, der findes i frø af marietidsel. Det er blevet vist in vitro og in vivo at hæmme PCa-vækst ved at målrette epidermal vækstfaktorreceptor (EGFR), IGF-1-receptor (IGF-1R) og nuklear faktor-kappa B (NF-kB) veje [133,134]. En nylig undersøgelse viste, at silibinin kan være nyttig i PCa-forebyggelse ved at hæmme TGF?2-ekspression og cancerassocierede fibroblast (CAF)-lignende biomarkører i de humane prostata-stromale celler [135]. Således er silibinin en lovende kandidat som et PCa kemopræventive middel, der afventer yderligere forskning.
Curcumin bruges som fødevaretilsætningsstof i Asien og som urtemedicin mod betændelse [136]. In vitro hæmmer curcumin det pro-inflammatoriske protein NF-?B, mens det inducerer apoptose gennem øget ekspression af proapoptotiske gener [137]. In vivo bremser curcumin PCa-vækst i mus, mens det sensibiliserer tumorer over for kemo- og radioterapier [136]; dog har intet menneskeligt forsøg undersøgt dets indvirkning på PCa.
Granatæble
Skallen og frugten af granatæbler og valnødder er rig på ellagitanniner (punicalaginer). Disse fytokemikalier metaboliseres let til den aktive form ellaginsyre af tarmfloraen [138]. Prækliniske eksperimenter viser, at ellagitanniner hæmmer PCa-proliferation og angiogenese under hypoxiske forhold og inducerer apoptose [137,138]. I prospektive forsøg med mænd med stigende PSA efter primær behandling, øgede granatæblejuice eller POMx, et kommercielt tilgængeligt granatæbleekstrakt, PSA-fordoblingstiden i forhold til baseline [139,140], selvom ingen forsøg inkluderede en placebogruppe. Resultater afventer fra en potentiel placebo-RCT, der bruger granatæbleekstrakt hos mænd med stigende PSA. I et placebokontrolleret forsøg havde to piller POMx dagligt i op til fire uger før radikal prostatektomi imidlertid ingen indflydelse på tumorpatologi eller oxidativ stress eller andre tumorforanstaltninger [141].
Grøn te
Grøn te indeholder en række antioxidante polyfenoler, herunder katekiner, såsom epigallocatechin gallat (EGCG), epigallocatechin (EGC), (?)-epicatechin-3-gallate (ECG) og (?)-epicatechin. Prækliniske undersøgelser tyder på, at EGCG hæmmer PCa-vækst, inducerer iboende og ydre apoptotiske veje og mindsker inflammation ved at hæmme NFkB [137]. Desuden er antioxidantegenskaberne af EGCG 25 til 100 gange mere potente end vitamin C og E [131]. I et prospektivt randomiseret præprostatektomiforsøg indtog mænd, der indtog brygget grøn te Lin et al. BMC Medicine (2015) 13:3 Side 7 af 15 før operationen havde øgede niveauer af grøn te polyfenoler i deres prostatavæv [142]. I et lille proof-of-principle forsøg med 60 mænd reducerede dagligt tilskud af 600 mg grøn te catechin-ekstrakt PCa-forekomsten med 90% (3% versus 30% i placebogruppen) [143]. Et andet lille forsøg viste også, at EGCG-tilskud resulterede i en signifikant reduktion i PSA, hepatocytvækstfaktor og vaskulær endotelvækstfaktor hos mænd med PCa [144]. Disse undersøgelser tyder på, at grøn te-polyfenoler kan sænke PCa-forekomsten og reducere PCa-progression, men mere forskning er nødvendig for at bekræfte og afklare dens mekanisme [137,143,145].
Resveratrol
Mens de fleste in vitro undersøgelser tyder på, at resveratrol hæmmer PCa-vækst [146-148], undertrykker resveratrol tumorvækst i nogle [137], men ikke alle dyremodeller [149], muligvis på grund af begrænset biotilgængelighed [150,151]. Til dato er der ingen kliniske forsøg, der undersøger de forebyggende eller terapeutiske virkninger af resveratrol på PCa.
Zyflamend
Zyflamend er en anti-inflammatorisk blanding af urter, der har vist sig at reducere PCa-progression ved at sænke ekspressionen af markører, herunder pAKT, PSA, histon-deacetylaser og androgenreceptor i dyremodeller og PCa-cellelinje [152-154]. På trods af dets anti-cancer potentiale [155] er meget få undersøgelser blevet udført på mennesker [156,157]. I et åbent fase I forsøg med 23 patienter med højgradig prostata intraepitelial neoplasi reducerede Zyflamend alene eller sammen med andre kosttilskud i 18 måneder risikoen for at udvikle PCa [156]. Flere RCT'er hos mennesker er nødvendige for at bekræfte effektiviteten og den kliniske anvendelse af dette urtetilskud.
Andre Whole Foods Frugt og grøntsager
Frugt og grøntsager er rige kilder til vitaminer, mineraler og fytokemikalier. Adskillige epidemiologiske undersøgelser fandt omvendte sammenhænge mellem totalt frugt- og grøntsagsindtag [158] og indtag af korsblomstrede grøntsager og PCa-risiko [159,160]. Allium-grøntsager, såsom hvidløg, porrer, purløg og skalotteløg, indeholder flere svovlholdige fytokemikalier, der blev foreslået for at forbedre immunsystemet, hæmme cellevækst, modulere ekspression af androgen-responsive gener og inducere apoptose [161]. Selvom antallet af publicerede undersøgelser er begrænset, tyder både prækliniske og epidemiologiske data på, at grøntsagsindtagelse af allium kan være beskyttende mod PCa, især lokaliseret sygdom [162]. Et randomiseret forsøg med 199 mænd fandt også, at et blandingstilskud af granatæble, grøn te, broccoli og gurkemeje signifikant reducerede stigningen i PSA hos mænd med PCa [163].
Tomater og tomatprodukter
En række undersøgelser har undersøgt sammenhængen mellem tomater og tomatprodukter med PCa, men resultaterne er ikke entydige. Antioxidanten lycopen, som er rig på tomater, er også blevet undersøgt specifikt for dens indvirkning på PCa. In vitro standser lycopen cellecyklussen i flere PCa-cellelinjer og reducerer IGF-1-signalering ved at inducere IGF-1-bindende proteiner [131]. Mens nogle dyreforsøg fandt, at lycopen specifikt bremser PCa-vækst [164] eller reducerer PCa-epitelceller i stadier af initiering, promovering og progression [165], fandt to undersøgelser modstridende fund mellem tomatpasta og lycopen [166,167]. Prospektive humane undersøgelser viste, at højere lycopenforbrug [168,169] eller højere serumniveauer var forbundet med lavere PCa-risiko [170], men andre har ikke [171,172]. Prostatalycopenkoncentration under en tærskel på 1 ng/mg var forbundet med PCa ved seks måneders opfølgningsbiopsi (P = 0.003) [173]. To kortsigtede præprostatektomiforsøg med tomatsauce eller lycopentilskud viste lycopenoptagelse i prostatavæv og antioxidant- og potentielle anticancereffekter [174,175]. Mens flere kliniske forsøg antydede et omvendt forhold mellem lycopentilskud, PSA-niveauer og fald i kræftrelaterede symptomer [171,176], har ingen storstilet randomiserede forsøg testet rollen af lycopen eller tomatprodukter i PCa-forebyggelse eller -behandling.
Kaffe
Kaffe indeholder koffein og flere uidentificerede phenolforbindelser, der kan tjene som antioxidanter. Epidemiologiske undersøgelser tyder på et omvendt forhold mellem kaffeforbrug og PCa-risiko, hovedsageligt for fremskreden eller dødelig sygdom, og resultaterne var uafhængige af koffeinindhold [177,178]. Selvom flere epidemiologiske undersøgelser [179-182] ikke fandt nogen sammenhæng mellem kaffeforbrug og PCa-risiko, konkluderede en nylig metaanalyse af prospektive undersøgelser, at kaffeforbrug kan reducere PCa-risikoen [183]. Den eller de potentielle involverede mekanismer og veje er ukendte, men kan omfatte antioxidanter, antiinflammatoriske virkninger, glukose- og insulinmetabolisme og potentiel indvirkning på IGF-I og cirkulerende kønshormoner.
Kostmønstre
Selvom mange enkelte næringsstoffer eller fødevarefaktorer er blevet undersøgt for deres indvirkning eller sammenhæng med PCa-risiko eller progression, har resultaterne stort set været inkonklusive. En potentiel årsag til inkonsistensen er det faktum, at påvirkningen af enkelt næringsstof eller fødevarefaktor kan være for lille til at blive opdaget. Derudover er næringsstoffer, der findes naturligt i fødevarer, ofte meget korrelerede og kan interagere med hinanden og dermed påvirke indvirkningen på PCa. Kostmønsteranalyse har således fået en stigende Lin et al. BMC Medicine (2015) 13:3 Side 8 af 15 men forskningen har været begrænset, og de eksisterende resultater har været inkonklusive. I en kohorte på 293,464 mænd var en høj diætkvalitet, som angivet af Healthy Eating Index (HEI)-score, forbundet med en lavere risiko for total PCa-risiko [70]. Middelhavsdiæten, som er høj i grøntsager, olivenolie, komplekse kulhydrater, magert kød og antioxidanter, anbefales konsekvent til patienter til forebyggelse af hjertekarsygdomme og fedme [184], og kan vise lovende i PCa-forebyggelse [185]. Fisk og omega-3 fedtsyreforbrug i middelhavsmønsteret var signifikant og omvendt forbundet med dødelig PCa-risiko. Derudover var overholdelse af middelhavsdiæten efter diagnosen ikke-metastatisk PCa forbundet med lavere overordnet dødelighed [186]. Hvorimod et vestligt mønster med højt indtag af rødt kød, forarbejdet kød, stegt fisk, chips, mælk med højt fedtindhold og hvidt brød var forbundet med en højere risiko for PCa [187].
Ydermere har asiatiske lande med højt forbrug af omega-3 PUFA'er, soja- og grøn te-baserede fytokemikalier, lavere PCa-forekomster sammenlignet med lande, der indtager en "vestlig-stil" diæt [188]. Imidlertid understøttede ikke alle undersøgelser [189-191] en sammenhæng mellem et bestemt kostmønster og risiko for PCa. Det er muligt, at den metode, der er brugt til at identificere kostmønstre, måske ikke har fanget alle de kostfaktorer, der er forbundet med PCa-risiko. Alternativt kan hvert kostmønster indeholde både gavnlige og skadelige komponenter, hvilket resulterer i en overordnet nulassociation. Mere forskning er nødvendig for at fortsætte med at søge efter kostmønstre, der kombinerer de fleste af de gavnlige næringsstoffer/fødefaktorer til PCa og begrænser de fleste af de negative næringsstoffer/fødevarefaktorer.
Fremtidig retning for kliniske forsøg
Baseret på de mange epidemiologiske, prækliniske og kliniske forsøg, der er beskrevet i denne gennemgang, lover diætinterventioner til forebyggelse og behandling af PCa stort. Derudover kan flere kostfaktorer og vitaminer/tilskud være forbundet med PCa-risiko og/eller sygdomsprogression. Prospektive randomiserede forsøg er klart indiceret for at identificere specifikke næringsstoffer eller kombinationsterapier til forebyggelse og behandling af PCa.
For nylig er aktiv overvågning (AS) dukket op som en levedygtig mulighed for mænd med lavere risiko for PCa. Mænd på AS er motiverede til at følge kost- og livsstilsændringer [192], hvilket gør denne delmængde til et godt mål for diætintervention og livskvalitetsforsøg [193]. PCa-overlevere, der er mere aktive og rapporterer "sunde" spisevaner (det vil sige indtagelse af fedtfattige, lavraffinerede kulhydratdiæter rig på frugt og grøntsager) har bedre overordnet livskvalitet sammenlignet med deres inaktive, usunde modstykker [194]. Således er flere randomiserede forsøg berettiget til at bestemme de overordnede langsigtede virkninger af diætintervention i denne population. Specifikt er nøglespørgsmål, der skal behandles i fremtidige forsøg: 1) Kan diætinterventioner forsinke behovet for behandling hos mænd med AS; 2) Kan diætinterventioner forhindre tilbagefald for mænd efter behandling; 3) Kan diætinterventioner forsinke progression blandt mænd med tilbagevendende sygdom og dermed forsinke behovet for hormonbehandling; 4) Kan diætinterventioner reducere bivirkningerne af PCa-behandlinger, herunder hormonbehandling og nyere målrettede terapier; og 5) Er der nogen rolle for diætinterventioner alene eller kombineret med målrettede terapier hos mænd i hormonbehandling for at forhindre kastratresistens eller efter fremkomsten af kastratresistenssygdom? Fordi stigende beviser viser, at metaboliske abnormiteter øger risikoen for PCa, er livsstilsintervention, der forbedrer den metaboliske profil, en win-win mulighed for PCa-forebyggelse og behandling [195,196].
Konklusioner: Prostatakræft
Fremtidig forskning er påkrævet for at bestemme den ideelle diæt til PCa-forebyggelse eller behandling. Men adskillige kostfaktorer og nogle kostmønstre lover at reducere PCa-risiko eller progression og er i overensstemmelse med nuværende kostråd for amerikanere [197]. Til rådgivning af patienter om diæt til primær og sekundær PCa-forebyggelse, mener mange, at hjertesund er lig med prostatasund.� Givet de nuværende inkonklusive resultater synes de bedste kostråd til forebyggelse eller behandling af PCa således at omfatte: øget frugt og grøntsager, udskiftning af raffineret kulhydrater med fuldkorn, reducere totalt og mættet fedt, reducere overstegt kød og indtage en moderat mængde kalorier eller reducere kulhydrater med et primært mål om at opnå og opretholde en sund kropsvægt.
Konkurrerende interesser Forfatterne erklærer, at de ikke har nogen konkurrerende interesser.
Forfatternes bidrag P-HL og SF udførte gennemgangen, P-HL udarbejdede manuskriptet og SF og WA redigerede og leverede kritisk input. Alle forfattere læste og godkendte det endelige manuskript.
Anerkendelser Finansieringen blev leveret af tilskud 1K24CA160653 (Freedland), NIH P50CA92131 (W. Aronson). Dette manuskript er resultatet af arbejde støttet med ressourcer og brugen af faciliteter på Veterans Administration Medical Center, West Los Angeles (W. Aronson).
Forfatteroplysninger 1 Department of Medicine, Division of Nephrology, Duke University Medical Center, Box 3487, Durham, NC 27710, USA. 2 Urology Section, Department of Surgery, Veterans Affairs Greater Los Angeles Healthcare System, Los Angeles, CA, USA. 3 Department of Urology, UCLA School of Medicine, Los Angeles, CA, USA. 4 Urology Section, Department of Surgery, Durham Veterans Affairs Medical Center, Division of Urology, Durham, NC, USA. 5 Duke Prostate Center, afdelinger for kirurgi og patologi, Duke University Medical Center, Durham, NC, USA.
blank
Referencer:
1. Center MM, Jemal A, Lortet-Tieulent J, Ward E, Ferlay J, Brawley O, Bray F:
International variation i forekomst af prostatacancer og dødelighed.
Eur Urol 2012, 61:1079�1092.
2. Masko EM, Allott EH, Freedland SJ: Forholdet mellem ernæring og
prostatakræft: er mere altid bedre? Eur Urol 2013, 63:810�820.
3. Mavropoulos JC, Isaacs WB, Pizzo SV, Freedland SJ: Er der en rolle for en
ketogen diæt med lavt kulhydratindhold i behandlingen af prostatacancer?
Urology 2006, 68:15-18.
4. Freedland SJ, Mavropoulos J, Wang A, Darshan M, Demark-Wahnefried W,
Aronson WJ, Cohen P, Hwang D, Peterson B, Fields T, Pizzo SV, Isaacs WB:
Kulhydratbegrænsning, vækst af prostatacancer og det insulinlignende
vækstfaktorakse. Prostata 2008, 68:11�19.
5. Mavropoulos JC: Buschemeyer VM 3., Tewari AK, Rokhfeld D, Pollak M,
Zhao Y, Febbo PG, Cohen P, Hwang D, Devi G, Demark-Wahnefried W,
Westman EC, Peterson BL, Pizzo SV, Freedland SJ: Effekterne af at variere
kostens kulhydrat- og fedtindhold på overlevelse i en murin LNCaP
prostatacancer xenograft model. Cancer Prev Res (Phila Pa) 2009,
2: 557 565.
6. Masko EM, Thomas JA 2., Antonelli JA, Lloyd JC, Phillips TE, Poulton SH,
Dewhirst MW, Pizzo SV, Freedland SJ: Lav-kulhydrat diæter og
prostatacancer: hvor lavt er �lavt nok�? Cancer Prev Res (Phila) 2010,
3: 1124 1131.
7. Drake I, Sonestedt E, Gullberg B, Ahlgren G, Bjartell A, Wallstrom P, Wirf�lt E:
Kostindtag af kulhydrater i forhold til risiko for prostatacancer: a
prospektiv undersøgelse i Malmø Diet and Cancer-kohorten. Am J Clin Nutr
2012, 96:1409�1418.
8. Zhang J, Shen C, Wang L, Ma Q, Xia P, Qi M, Yang M, Han B: Metformin
hæmmer epitel-mesenkymal overgang i prostatacancerceller:
Involvering af tumorsuppressoren miR30a og dets målgen SOX4.
Biochem Biophys Res Commun 2014, 452:746�752.
9. Lee SY, Song CH, Xie YB, Jung C, Choi HS, Lee K: SMILE opreguleret af
metformin hæmmer funktionen af androgenreceptor i prostatacancer
celler. Cancer Lett 2014, 354:390�397.
10. Demir U, Koehler A, Schneider R, Schweiger S, Klocker H: Metformin antitumor
effekt via forstyrrelse af MID1 translationsregulatorkomplekset
og AR-nedregulering i prostatacancerceller. BMC Cancer 2014, 14:52.
11. Margel D: Metformin til forebyggelse af prostatacancer: en opfordring til at forene. Eur Urol
2014. doi:10.1016/j.eururo.2014.05.012. [Epub før tid]
12. Margel D, Urbach DR, Lipscombe LL, Bell CM, Kulkarni G, Austin PC, Fleshner
N: Metforminbrug og alle årsager og prostatacancer-specifik dødelighed
blandt mænd med diabetes. J Clin Oncol 2013, 31:3069�3075.
13. Tseng CH: Metformin reducerer risikoen for prostatacancer betydeligt
hos taiwanske mænd med type 2-diabetes mellitus. Eur J Cancer 2014,
50: 2831 2837.
14. Joshua AM, Zannella VE, Downes MR, Bowes B, Hersey K, Koritzinsky M,
Schwab M, Hofmann U, Evans A, van der Kwast T, Trachtenberg J, Finelli A,
Fleshner N, Sweet J, Pollak M: Et pilotvindue med muligheder
neoadjuverende undersøgelse af metformin i lokaliseret prostatacancer. Prostata
Cancer Prostatic Dis 2014, 17:252�258.
15. Rothermundt C, Hayoz S, Templeton AJ, Winterhalder R, Strebel RT, Bartschi
D, Pollak M, Lui L, Endt K, Schiess R, R�schoff JH, Cathomas R, Gillessen S:
Metformin i kemoterapi-naiv kastrationsresistent prostatakræft:
Et multicenter fase 2 forsøg (SAKK 08/09). Eur Urol 2014, 66:468�474.
16. Allott EH, Abern MR, Gerber L, Keto CJ, Aronson WJ, Terris MK, Kane CJ,
Amling CL, Cooperberg MR, Moorman PG, Freedland SJ: Metformin gør
påvirker ikke risikoen for biokemisk tilbagefald efter radikal
prostatektomi: resultater fra SEARCH-databasen. Prostatakræft
Prostatic Dis 2013, 16:391�397.
17. Rieken M, Kluth LA, Xylinas E, Fajkovic H, Becker A, Karakiewicz PI, Herman
M, Lotan Y, Seitz C, Schramek P, Remzi M, Loidl W, Pummer K, Lee RK,
Faison T, Scherr DS, Kautzky-Willer A, Bachmann A, Tewari A, Shariat SF:
Sammenslutning af diabetes mellitus og metformin brug med biokemisk
recidiv hos patienter behandlet med radikal prostatektomi for prostata
Kræft. World J Urol 2014, 32:999�1005.
18. Margel D, Urbach D, Lipscombe LL, Bell CM, Kulkarni G, Austin PC, Fleshner
N: Sammenhæng mellem metforminbrug og risiko for prostatacancer og
dens karakter. J Natl Cancer Inst 2013, 105:1123�1131.
19. Franciosi M, Lucisano G, Lapice E, Strippoli GF, Pellegrini F, Nicolucci A:
Metforminbehandling og risiko for kræft hos patienter med type 2-diabetes:
systematisk gennemgang. PLoS One 2013, 8:e71583.
20. Kaushik D, Karnes RJ, Eisenberg MS, Rangel LJ, Carlson RE, Bergstralh EJ:
Effekt af metformin på prostatacancer udfald efter radikal
prostatektomi. Urol Oncol 2014, 32:43 e41�47.
21. Bensimon L, Yin H, Suissa S, Pollak MN, Azoulay L: Brugen af metformin i
patienter med prostatakræft og risiko for død. Kræftepidemiol
Biomarkører Prev 2014, 23:2111�2118.
22. Tsilidis KK, Capothanassi D, Allen NE, Rizos EC, Lopez DS, van Veldhoven K,
Sacerdote C, Ashby D, Vineis P, Tzoulaki I, Ioannidis JP: Metformin gør ikke
påvirke kræftrisiko: en kohorteundersøgelse i UK Clinical Practice Research
Datalink analyseret som en intention-to-treat-forsøg. Diabetespleje 2014,
37: 2522 2532.
23. Levine ME, Suarez JA, Brandhorst S, Balasubramanian P, Cheng CW, Madia F,
Fontana L, Mirisola MG, Guevara-Aguirre J, Wan J, Passarino G, Kennedy BK,
Wei M, Cohen P, Crimmins EM, Longo VD: Lavt proteinindtag er forbundet
med en væsentlig reduktion i IGF-1, kræft og overordnet dødelighed hos de 65
og yngre, men ikke ældre befolkning. Cell Metab 2014, 19:407�417.
24. Solon-Biet SM, McMahon AC, Ballard JW, Ruohonen K, Wu LE, Cogger VC,
Warren A, Huang X, Pichaud N, Melvin RG, Gokarn R, Khalil M, Turner N,
Cooney GJ, Sinclair DA, Raubenheimer D, Le Couteur DG, Simpson SJ:
forholdet mellem makronæringsstoffer, ikke kalorieindtag, dikterer kardiometabolisk
sundhed, aldring og lang levetid hos ad libitum-fodrede mus. Cell Metab 2014,
19: 418 430.
25. Richman EL, Stampfer MJ, Paciorek A, Broering JM, Carroll PR, Chan JM:
Indtag af kød, fisk, fjerkræ og æg og risiko for prostatakræft
progression. Am J Clin Nutr 2010, 91:712�721.
26. Joshi AD, John EM, Koo J, Ingles SA, Stern MC: Fiskeindtag, madlavning
praksis og risiko for prostatacancer: resultater fra en multietnisk
case�kontrolundersøgelse. Cancer Causes Control 2012, 23:405�420.
27. Joshi AD, Corral R, Catsburg C, Lewinger JP, Koo J, John EM, Ingles SA,
Stern MC: Rødt kød og fjerkræ, madlavningspraksis, genetisk modtagelighed
og risiko for prostatacancer: resultater fra en multietnisk tilfældekontrol
undersøgelse. Carcinogenese 2012, 33:2108�2118.
28. Catsburg C, Joshi AD, Corral R, Lewinger JP, Koo J, John EM, Ingles SA,
Stern MC: Polymorfismer i carcinogen metabolisme enzymer, fisk
indtag og risiko for prostatakræft. Carcinogenese 2012, 33:1352-1359.
29. Pettersson A, Kasperzyk JL, Kenfield SA, Richman EL, Chan JM, Willett WC,
Stampfer MJ, Mucci LA, Giovannucci EL: Mælke- og mejeriforbrug
blandt mænd med prostatakræft og risiko for metastaser og prostata
kræftdød. Cancer Epidemiol Biomarkers Prev 2012, 21:428�436.
30. Deneo-Pellegrini H, Ronco AL, De Stefani E, Boffetta P, Correa P,
Mendilaharsu M, Acosta G: Fødevaregrupper og risiko for prostatacancer: a
case�kontrolundersøgelse i Uruguay. Cancer Causes Control 2012, 23:1031�1038.
31. Park SY, Murphy SP, Wilkens LR, Stram DO, Henderson BE, Kolonel LN:
Calcium, D-vitamin og mejeriprodukter og risiko for prostatakræft:
den multietniske kohorteundersøgelse. Am J Epidemiol 2007, 166:1259-1269.
32. Song Y, Chavarro JE, Cao Y, Qiu W, Mucci L, Sesso HD, Stampfer MJ,
Giovannucci E, Pollak M, Liu S, Ma J: Indtagelse af sødmælk er forbundet med
prostatacancer-specifik dødelighed blandt amerikanske mandlige læger. J Nutr feb
2013, 143:189�196.
33. Young NJ, Metcalfe C, Gunnell D, Rowlands MA, Lane JA, Gilbert R, Avery
KN, Davis M, Neal DE, Hamdy FC, Donovan J, Martin RM, Holly JM: Et tværsnit
analyse af sammenhængen mellem kost og insulinlignende vækst
faktor (IGF)-I, IGF-II, IGF-bindende protein (IGFBP)-2 og IGFBP-3 hos mænd i
Det Forenede Kongerige. Cancer Causes Control 2012, 23:907�917.
34. Christensen MJ, Quiner TE, Nakken HL, Lephart ED, Eggett DL, Urie PM:
Kombinationseffekter af diætsoja og methylselenocystein i en mus
model for prostatakræft. Prostata 2013, 73:986�995.
35. Bosland MC, Kato I, Zeleniuch-Jacquotte A, Schmoll J, Enk Rueter E,
Melamed J, Kong MX, Macias V, Kajdacsy-Balla A, Lumey LH, Xie H, Gao W,
Walden P, Lepor H, Taneja SS, Randolph C, Schlicht MJ, Meserve-Watanabe
H, Deaton RJ, Davies JA: Effekt af sojaproteinisolattilskud på
biokemisk recidiv af prostatacancer efter radikal prostatektomi: a
randomiseret forsøg. JAMA 2013, 310:170�178.
36. Chiyomaru T, Yamamura S, Fukuhara S, Yoshino H, Kinoshita T, Majid S, Saini
S, Chang I, Tanaka Y, Enokida H, Seki N, Nakagawa M, Dahiya R: Genistein
hæmmer prostatacancer cellevækst ved at målrette mod miR-34a og onkogen
VARM LUFT. PLoS One 2013, 8:e70372.
37. Zhang S, Wang Y, Chen Z, Kim S, Iqbal S, Chi A, Ritenour C, Wang YA, Kucuk
O, Wu D: Genistein øger effektiviteten af cabazitaxel kemoterapi
i metastatiske kastrationsresistente prostatacancerceller. Prostata 2013,
73:1681-1689.38. van Die MD, Bone KM, Williams SG, Pirotta MV: Soja- og sojaisoflavoner i
prostatacancer: en systematisk gennemgang og meta-analyse af randomiserede
kontrollerede forsøg. BJU Int 2014, 113:E119�E130.
39. Hamilton-Reeves JM, Banerjee S, Banerjee SK, Holzbeierlein JM, Thrasher JB,
Kambhampati S, Keighley J, Van Veldhuizen P: Kortvarig sojaisoflavon
intervention hos patienter med lokaliseret prostatacancer: en randomiseret,
dobbeltblindet, placebokontrolleret forsøg. PLoS One 2013, 8:e68331.
40. Pavese JM, Krishna SN, Bergan RC: Genistein hæmmer human prostata
kræftcelleløsning, invasion og metastasering. Am J Clin Nutr 2014,
100:431S�436S.
41. Gonzalez-Menendez P, Hevia D, Rodriguez-Garcia A, Mayo JC, Sainz RM:
Regulering af GLUT-transportører af flavonoider i androgenfølsomme og
-ufølsomme prostatacancerceller. Endocrinology 2014, 155:3238�3250.
42. Hirata H, Hinoda Y, Shahryari V, Deng G, Tanaka Y, Tabatabai ZL, Dahiya R:
Genistein nedregulerer onco-miR-1260b og opregulerer sFRP1 og
Smad4 via demethylering og histonmodifikation i prostatacancer
celler. Br J Cancer 2014, 110:1645-1654.
43. Handayani R, Rice L, Cui Y, Medrano TA, Samedi VG, Baker HV, Szabo NJ,
Shiverick KT: Sojaisoflavoner ændrer ekspression af gener forbundet med
cancerprogression, herunder interleukin-8, hos androgen-uafhængige
PC-3 humane prostatacancerceller. J Nutr 2006, 136:75�82.
44. Travis RC, Allen NE, Appleby PN, Price A, Kaaks R, Chang-Claude J, Boeing H,
Aleksandrova K, Tjanneland A, Johnsen NF, Overvad K, Ramn Quirs J,
Gonz�lez CA, Molina-Montes E, S�nchez MJ, Larra�aga N, Casta�o JM,
Ardanaz E, Khaw KT, Wareham N, Trichopoulou A, Karapetyan T, Rafnsson
SB, Palli D, Krogh V, Tumino R, Vineis P, Bueno-de-Mesquita HB, Stattin P,
Johansson M, et al: Prædiagnostiske koncentrationer af plasma genistein og
risiko for prostatacancer hos 1,605 mænd med prostatakræft og 1,697
matchede kontroldeltagere i EPIC. Cancer Causes Control 2012,
23: 1163 1171.
45. Jackson MD, McFarlane-Anderson ND, Simon GA, Bennett FI, Walker SP:
Urinary phytoøstrogener og risiko for prostatakræft hos jamaicanske mænd.
Cancer Causes Control 2010, 21:2249�2257.
46. Lazarevic B, Hammarström C, Yang J, Ramberg H, Diep LM, Karlsen SJ,
Kucuk O, Saatcioglu F, Task�n KA, Svindland A: Effekterne af kortsigtet
genistein intervention på prostata biomarkør ekspression hos patienter med
lokaliseret prostatacancer før radikal prostatektomi. Br J Nutr 2012,
108: 2138 2147.
47. Epstein MM, Kasperzyk JL, Mucci LA, Giovannucci E, Price A, Wolk A,
H�kansson N, Fall K, Andersson SO, Andr�n O: Kostens fedtsyreindtag og
overlevelse af prostatacancer i Örebro län, Sverige. Am J Epidemiol 2012,
176: 240 252.
48. Kobayashi N, Barnard RJ, Said J, Hong-Gonzalez J, Corman DM, Ku M,
Doan NB, Gui D, Elashoff D, Cohen P, Aronson WJ: Effekt af fedtfattig kost på
udvikling af prostatacancer og Akt-phosphorylering i Hi-Myc
transgen musemodel. Cancer Res 2008, 68:3066�3073.
49. Ngo TH, Barnard RJ, Cohen P, Freedland S, Tran C, deGregorio F, Elshimali
YI, Heber D, Aronson WJ: Effekt af isokalorisk fedtfattig kost på mennesker
LAPC-4 prostatacancer xenotransplantater i svær kombineret immundefekt
mus og den insulinlignende vækstfaktorakse. Clin Cancer Res 2003,
9: 2734 2743.
50. Huang M, Narita S, Numakura K, Tsuruta H, Saito M, Inoue T, Horikawa Y,
Tsuchiya N, Habuchi T: En diæt med højt fedtindhold øger spredning af
prostatacancerceller og aktiverer MCP-1/CCR2-signalering. Prostata 2012,
72: 1779 1788.
51. Chang SN, Han J, Abdelkader TS, Kim TH, Lee JM, Song J, Kim KS, Park JH,
Park JH: Højt indtag af animalsk fedt øger prostatacancerprogressionen
og reducerer glutathionperoxidase 3-ekspression i tidlige stadier af
TAMP mus. Prostata 2014, 74:1266�1277.
52. Bidoli E, Talamini R, Bosetti C, Negri E, Maruzzi D, Montella M, Franceschi S,
La Vecchia C: Makronæringsstoffer, fedtsyrer, kolesterol og prostatacancer
risiko. Ann Oncol 2005, 16:152-157.
53. Park SY, Murphy SP, Wilkens LR, Henderson BE, Kolonel LN: Fedt og kød
indtag og risiko for prostatacancer: det multietniske kohortestudie. Int J Kræft
2007, 121:1339�1345.
54. Wallstrom P, Bjartell A, Gullberg B, Olsson H, Wirfalt E: En prospektiv undersøgelse
om kostfedt og forekomst af prostatacancer (Malmø, Sverige).
Cancer Causes Control 2007, 18:1107�1121.
55. Crowe FL, Key TJ, Appleby PN, Travis RC, Overvad K, Jakobsen MU,
Johnsen NF, Tjanneland A, Linseisen J, Rohrmann S, Boeing H, Pischon T,
Trichopoulou A, Lagiou P, Trichopoulos D, Sacerdote C, Palli D, Tumino R,
Krogh V, Bueno-de-Mesquita HB, Kiemeney LA, Chirlaque MD, Ardanaz E,
S�nchez MJ, Larra�aga N, Gonz�lez CA, Quir�s JR, Manjer J, Wirf�lt E, Stattin
P, et al: Fedtindtag i kosten og risiko for prostatacancer i Europa
Prospektiv undersøgelse af kræft og ernæring. Am J Clin Nutr 2008,
87: 1405 1413.
56. Ohwaki K, Endo F, Kachi Y, Hattori K, Muraishi O, Nishikitani M, Yano E:
Forholdet mellem kostfaktorer og prostataspecifikt antigen i
sunde mænd. Urol Int 2012, 89:270�274.
57. Bassett JK, Severi G, Hodge AM, MacInnis RJ, Gibson RA, Hopper JL,
Engelsk DR, Giles GG: Plasma phospholipid fedtsyrer, diætiske fedtsyrer
og risiko for prostatacancer. Int J Cancer 2013, 133:1882-1891.
58. Richman EL, Kenfield SA, Chavarro JE, Stampfer MJ, Giovannucci EL, Willett
WC, Chan JM: Fedtindtag efter diagnose og risiko for dødelig prostatacancer
og dødelighed af alle årsager. JAMA Intern Med 2013, 173:1318�1326.
59. Williams CD, Whitley BM, Hoyo C, Grant DJ, Iraggi JD, Newman KA, Gerber
L, Taylor LA, McKeever MG, Freedland SJ: Et højt forhold mellem diæt n-6/n-3
flerumættede fedtsyrer er forbundet med øget risiko for prostata
Kræft. Nutr Res 2011, 31:1�8.
60. Chua ME, Sio MC, Sorongon MC, Dy JS: Sammenhæng mellem diætindtagelse af
omega-3 og omega-6 fedtsyrer med risiko for prostatakræft
udvikling: en meta-analyse af prospektive studier og gennemgang af
litteratur. Prostatakræft 2012, 2012:826254.
61. Berquin IM, Edwards IJ, Kridel SJ, Chen YQ: Flerumættet fedtsyre
stofskifte ved prostatacancer. Cancer Metastasis Rev 2011, 30:295-309.
62. Aronson WJ, Kobayashi N, Barnard RJ, Henning S, Huang M, Jardack PM, Liu
B, Gray A, Wan J, Konijeti R, Freedland SJ, Castor B, Heber D, Elashoff D, Said
J, Cohen P, Galet C: Fase II prospektivt randomiseret forsøg med en fedtfattig diæt
med fiskeolietilskud hos mænd, der gennemgår radikal prostatektomi.
Cancer Prev Res (Phila) 2011, 4:2062�2071.
63. Hughes-Fulford M, Li CF, Boonyaratanakornkit J, Sayyah S: Arachidonsyre
aktiverer phosphatidylinositol 3-kinase signalering og inducerer gen
udtryk i prostatacancer. Cancer Res 2006, 66:1427-1433.
64. Moreel X, Allaire J, Leger C, Caron A, Labonte ME, Lamarche B, Julien P,
Desmeules P, T�tu B, Fradet V: Prostata- og omega-3-fedtsyrer via kosten
og prostatacancerprogression under aktiv overvågning. Kræft Forrige
Res (Phila) 2014, 7:766�776.
65. Spencer L, Mann C, Metcalfe M, Webb M, Pollard C, Spencer D, Berry D,
Steward W, Dennison A: Effekten af omega-3 FA'er på tumorangiogenese
og deres terapeutiske potentiale. Eur J Cancer 2009, 45:2077�2086.
66. Gu Z, Suburu J, Chen H, Chen YQ: Mekanismer for omega-3 flerumættede
fedtsyrer i forebyggelse af prostatacancer. Biomed Res Int 2013, 2013:824563.
67. Lloyd JC, Masko EM, Wu C, Keenan MM, Pilla DM, Aronson WJ, Chi JT,
Freedland SJ: Fiskeolie bremser prostatacancer xenograft vækst i forhold til
andre diætfedtstoffer og er forbundet med nedsat mitokondrie og
insulin pathway genekspression. Prostatakræft Prostatasygdom 2013,
16: 285 291.
68. Williams CM, Burdge G: Langkædet n-3 PUFA: plante v. marine kilder.
Proc Nutr Soc 2006, 65:42�50.
69. Galet C, Gollapudi K, Stepanian S, Byrd JB, Henning SM, Grogan T, Elashoff
D, Heber D, Said J, Cohen P, Aronson WJ: Effekten af en fedtfattig fiskeoliediæt
på proinflammatoriske eicosanoider og cellecyklusprogressionsscore i
mænd, der gennemgår radikal prostatektomi. Cancer Prev Res (Phila) 2014,
7: 97 104.
70. Bosire C, Stampfer MJ, Subar AF, Park Y, Kirkpatrick SI, Chiuve SE, Hollenbeck
AR, Reedy J: Indeksbaserede kostmønstre og risikoen for prostatacancer
i NIH-AARP kost- og sundhedsundersøgelsen. Am J Epidemiol 2013, 177:504�513.
71. Aronson WJ, Barnard RJ, Freedland SJ, Henning S, Elashoff D, Jardack PM,
Cohen P, Heber D, Kobayashi N: Væksthæmmende effekt af fedtfattig kost
om prostatacancerceller: resultater af en potentiel, randomiseret kost
interventionsforsøg hos mænd med prostatacancer. J Urol 2010, 183:345�350.
72. Brouwer IA, Geleijnse JM, Klaasen VM, Smit LA, Giltay EJ, de Goede J,
Heijboer AC, Kromhout D, Katan MB: Effekt af alfa-linolensyre
tilskud på serum prostata specifikt antigen (PSA): resultater fra
alfa omega forsøget. PLoS One 2013, 8:e81519.
73. Chua ME, Sio MC, Sorongon MC, Morales ML Jr: Serums relevans
niveauer af langkædede omega-3 flerumættede fedtsyrer og prostata
kræftrisiko: En metaanalyse. Can Urol Assoc J 2013, 7:E333�E343.
74. Yue S, Li J, Lee SY, Lee HJ, Shao T, Song B, Cheng L, Masterson TA, Liu X,
Ratliff TL, Cheng JX: Kolesterylesterakkumulering induceret af PTEN-tab
og PI3K/AKT-aktivering ligger til grund for human prostatacancer
aggressivitet. Cell Metab 2014, 19:393�406.
75. Sun Y, Sukumaran P, Varma A, Derry S, Sahmoun AE, Singh BB: Kolesterolinduceret
aktivering af TRPM7 regulerer celleproliferation, migration,
og levedygtighed af humane prostataceller. Biochim Biophys Acta 1843,
2014: 1839 1850.
76. Murai T: Kolesterolsænkning: rolle i kræftforebyggelse og behandling.
Biol Chem 2014. doi:10.1515/hsz-2014-0194. [Epub før tid]
77. Zhuang L, Kim J, Adam RM, Solomon KR, Freeman MR: Kolesterol
målretning ændrer lipid-flådens sammensætning og celleoverlevelse ved prostatacancer
celler og xenotransplantater. J Clin Invest 2005, 115:959�968.
78. Mostaghel EA, Solomon KR, Pelton K, Freeman MR, Montgomery RB:
Indvirkning af cirkulerende kolesterolniveauer på vækst og intratumoral
androgenkoncentration af prostatatumorer. PLoS One 2012,
7: e30062.
79. Morote J, Celma A, Planas J, Placer J, de Torres I, Olivan M, Carles J,
Revent's J, Doll A: Serumkolesterol- og statinbrugs rolle i risikoen for
påvisning af prostatacancer og tumoraggressivitet. Int J Mol Sci 2014,
15: 13615 13623.
80. Allott EH, Howard LE, Cooperberg MR, Kane CJ, Aronson WJ, Terris MK,
Amling CL, Freedland SJ: Postoperativ statinbrug og risiko for biokemisk
tilbagefald efter radikal prostatektomi: resultater fra Shared
Equal Access Regional Cancer Hospital (SØG) database. BJU Int 2014,
114: 661 666.
81. Jespersen CG, Norgaard M, Friis S, Skriver C, Borre M: Statinbrug og risiko for
prostatacancer: Et dansk befolkningsbaseret case�kontrolstudie,
1997-2010. Cancer Epidemiol 2014, 38:42–47.
82. Meyers CD, Kashyap ML: Farmakologisk forhøjelse af højdensitet
lipoproteiner: nyere indsigt i virkningsmekanisme og åreforkalkning
beskyttelse. Curr Opin Cardiol 2004, 19:366-373.
83. Xia P, Vadas MA, Rye KA, Barter PJ, Gamble JR: Lipoproteiner med høj densitet
(HDL) afbryder sphingosinkinase-signalvejen. En mulig
mekanisme til beskyttelse mod aterosklerose ved HDL. J Biol Chem
1999, 274:33143�33147.
84. Kotani K, Sekine Y, Ishikawa S, Ikpot IZ, Suzuki K, Remaley AT: Højdensitet
lipoprotein og prostatacancer: en oversigt. J Epidemiol 2013,
23: 313 319.
85. Soni MG, Thurmond TS, Miller ER 3rd, Spriggs T, Bendich A, Omaye ST:
Sikkerhed af vitaminer og mineraler: kontroverser og perspektiv. Toxicol
Sci 2010, 118:348�355.
86. Neuhouser ML, Barnett MJ, Kristal AR, Ambrosone CB, King I, Thornquist M,
Goodman G: (n-6) PUFA-stigning og mejeriprodukter reducerer prostata
kræftrisiko hos storrygere. J Nutr 2007, 137:1821-1827.
87. Karppi J, Kurl S, Laukkanen JA, Kauhanen J: Serum beta-caroten i relation
til risiko for prostatacancer: Kuopio iskæmisk hjertesygdomsrisiko
Faktor undersøgelse. Nutr Cancer 2012, 64:361�367.
88. Margalit DN, Kasperzyk JL, Martin NE, Sesso HD, Gaziano JM, Ma J, Stampfer
MJ, Mucci LA: Brug af beta-carotenantioxidanter under strålebehandling
og prostatacancer udfald i lægernes sundhedsundersøgelse. Int J Radiat
Oncol Biol Phys 2012, 83:28�32.
89. Roswall N, Larsen SB, Friis S, Outzen M, Olsen A, Christensen J, Dragsted LO,
Tj�nneland A: Mikronæringsstofindtag og risiko for prostatacancer i en
årgang af midaldrende, danske mænd. Cancer Causes Control 2013,
24: 1129 1135.
90. Gilbert R, Metcalfe C, Fraser WD, Donovan J, Hamdy F, Neal DE, Lane JA,
Martin RM: Sammenslutninger af cirkulerende retinol, vitamin E og 1,25-
dihydroxyvitamin D med prostatacancer diagnose, stadium og grad.
Cancer Causes Control 2012, 23:1865�1873.
91. Bistulfi G, Foster BA, Karasik E, Gillard B, Miecznikowski J, Dhiman VK,
Smiraglia DJ: Diætisk folatmangel blokerer prostatacancerprogression
i TRAMP-modellen. Cancer Prev Res (Phila) 2011, 4:1825-1834.
92. Collin SM: Folat og B12 i prostatacancer. Adv Clin Chem 2013,
60: 1 63.
93. Tio M, Andrici J, Cox MR, Eslick GD: Folatindtag og risikoen for prostata
kræft: en systematisk gennemgang og metaanalyse. Prostatakræft Prostatakræft
Dis 2014, 17:213�219.
94. Vollset SE, Clarke R, Lewington S, Ebbing M, Halsey J, Lonn E, Armitage J,
Manson JE, Hankey GJ, Spence JD, Galan P, B�naa KH, Jamison R, Gaziano
JM, Guarino P, Baron JA, Logan RF, Giovannucci EL, den Heijer M, Ueland
PM, Bennett D, Collins R, Peto R, B-Vitamin Treatment Trialists' Collaboration:
Effekter af folinsyretilskud på overordnet og stedspecifik cancer
forekomst under de randomiserede forsøg: metaanalyser af data på 50,000
enkeltpersoner. Lancet 2013, 381:1029�1036.
95. Verhage BA, Cremers P, Schouten LJ, Goldbohm RA, van den Brandt PA:
Folat- og folatvitaminer i kosten og risikoen for prostatacancer
i det hollandske kohortestudie. Cancer Causes Control 2012,
23: 2003 2011.
96. Tavani A, Malerba S, Pelucchi C, Dal Maso L, Zucchetto A, Serraino D, Levi F,
Montella M, Franceschi S, Zambon A, La Vecchia C: Diætetiske folater og
kræftrisiko i et netværk af case-kontrolstudier. Ann Oncol 2012,
23: 2737 2742.
97. Moreira DM, Banez LL, Presti JC Jr, Aronson WJ, Terris MK, Kane CJ, Amling
CL, Freedland SJ: Højt serumfolat er forbundet med reduceret
biokemisk recidiv efter radikal prostatektomi: resultater fra
SØG Database. Int Braz J Urol 2013, 39:312�318. diskussion 319.
98. Han YY, Song JY, Talbott EO: Serumfolat og prostataspecifikt antigen i
De Forenede Stater. Cancer Causes Control 2013, 24:1595�1604.
99. Rycyna KJ, Bacich DJ, O'Keefe DS: Folats modsatte roller i prostata
Kræft. Urology 2013, 82:1197-1203.
100. Gilbert R, Martin RM, Beynon R, Harris R, Savovic J, Zuccolo L, Bekkering GE,
Fraser WD, Sterne JA, Metcalfe: Sammenslutninger af cirkulerende og diæt
D-vitamin med risiko for prostatacancer: en systematisk gennemgang og dosis�
respons meta-analyse. Cancer Causes Control 2011, 22:319�340.
101. Schenk JM, Till CA, Tangen CM, Goodman PJ, Song X, Torkko KC, Kristal AR,
Peters U, Neuhouser ML: Serum 25-hydroxyvitamin d koncentrationer og
risiko for prostatacancer: resultater fra forsøget med forebyggelse af prostatakræft.
Cancer Epidemiol Biomarkers Prev 2014, 23:1484�1493.
102. Schwartz GG: D-vitamin i blod og risiko for prostatacancer: lektioner
fra Selen og Vitamin E Cancer Prevention Trial og
Forsøg til forebyggelse af prostatacancer. Cancer Epidemiol Biomarkers Forrige 2014,
23: 1447 1449.
103. Giangreco AA, Vaishnav A, Wagner D, Finelli A, Fleshner N, Van der Kwast T,
Vieth R, Nonn L: Tumor suppressor mikroRNA'er, miR-100 og -125b, er
reguleret af 1,25-dihydroxyvitamin D i primære prostataceller og i
patientvæv. Cancer Prev Res (Phila) 2013, 6:483�494.
104. Hollis BW, Marshall DT, Savage SJ, Garrett-Mayer E, Kindy MS, Gattoni-Celli S:
D3-vitamintilskud, lavrisiko prostatacancer og sundhed
uligheder. J Steroid Biochem Mol Biol 2013, 136:233-237.
105. Sha J, Pan J, Ping P, Xuan H, Li D, Bo J, Liu D, Huang Y: Synergistisk effekt
og mekanisme for A-vitamin og D-vitamin til at inducere apoptose af
prostatacancerceller. Mol Biol Rep 2013, 40:2763-2768.
106. Chandler PD, Giovannucci EL, Scott JB, Bennett GG, Ng K, Chan AT, Hollis
BW, Emmons KM, Fuchs CS, Drake BF: Nul sammenhæng mellem D-vitamin
og PSA-niveauer blandt sorte mænd i et D-vitamintilskudsforsøg.
Cancer Epidemiol Biomarkers Prev 2014, 23:1944�1947.
107. Skaaby T, Husemoen LL, Thuesen BH, Pisinger C, Jorgensen T, Roswall N,
Larsen SC, Linneberg A: Prospektiv befolkningsbaseret undersøgelse af
sammenhæng mellem serum 25-hydroxyvitamin-D niveauer og
forekomst af specifikke typer kræft. Cancer Epidemiol Biomarkers Prev
2014, 23:1220�1229.
108. Holt SK, Kolb S, Fu R, Horst R, Feng Z, Stanford JL: Cirkulerende niveauer af
25-hydroxyvitamin D og prostatacancer prognose. Kræftepidemiol
2013, 37:666�670.
109. Wong YY, Hyde Z, McCaul KA, Yeap BB, Golledge J, Hankey GJ, Flicker L:
Hos ældre mænd er lavere plasma 25-hydroxyvitamin D forbundet med
reduceret forekomst af prostata, men ikke kolorektal eller lungekræft.
PLoS One 2014, 9:e99954.
110. Xu Y, Shao X, Yao Y, Xu L, Chang L, Jiang Z, Lin Z: Positiv association
mellem cirkulerende 25-hydroxyvitamin D-niveauer og risiko for prostatacancer:
nye resultater fra en opdateret metaanalyse. J Cancer Res Clin Oncol
2014, 140:1465�1477.
111. Meyer HE, Robsahm TE, Bjorge T, Brustad M, Blomhoff R: Vitamin D, sæson,
og risiko for prostatacancer: en indlejret case�kontrolundersøgelse inden for
Norske sundhedsstudier. Am J Clin Nutr 2013, 97:147�154.
112. Kristal AR, Till C, Song X, Tangen CM, Goodman PJ, Neuhauser ML, Schenk
JM, Thompson IM, Meyskens FL Jr, Goodman GE, Minasian LM, Parnes HL,
Klein EA: Plasma D-vitamin og prostatakræftrisiko: resultater fra
Selen og E-vitamin Kræftforebyggende forsøg. Kræftepidemiol
Biomarkører Prev 2014, 23:1494�1504.
113. Weinstein SJ, Mondul AM, Kopp W, Rager H, Virtamo J, Albanes D:
Cirkulerende 25-hydroxyvitamin D, vitamin D-bindende protein og risiko for
prostatakræft. Int J Cancer 2013, 132:2940�2947.
114. Guo Z, Wen J, Kan Q, Huang S, Liu X, Sun N, Li Z: Mangel på tilknytning
mellem vitamin D-receptorgenet FokI og BsmI polymorfismer og risiko for prostatacancer: en opdateret metaanalyse, der involverer 21,756 forsøgspersoner. Tumor Biol 2013, 34:3189�3200115. Wang L, Sesso HD, Glynn RJ, Christen WG, Bubes V, Manson JE, Buring JE,
Gaziano JM: Vitamin E og C tilskud og risiko for kræft hos mænd:
posttrial opfølgning i lægens sundhedsundersøgelse II randomiseret forsøg.
Am J Clin Nutr 2014, 100:915�923.
116. Virtamo J, Taylor PR, Kontto J, Mannisto S, Utriainen M, Weinstein SJ,
Huttunen J, Albanes D: Virkninger af alfa-tocopherol og beta-caroten
tilskud på kræftforekomst og dødelighed: 18 år
postintervention opfølgning af Alpha-tocopherol, Beta-caroten
Kræftforebyggende undersøgelse. Int J Cancer 2014, 135:178�185.
117. Basu A, Imrhan V: E-vitamin og prostatacancer: er E-vitamin succinat a
overlegen kemopræventive middel? Nutr Rev 2005, 63:247�251.
118. Lawson KA, Wright ME, Subar A, Mouw T, Hollenbeck A, Schatzkin A,
Leitzmann MF: Multivitaminbrug og risiko for prostatacancer i
National Institutes of Health-AARP kost- og sundhedsundersøgelse. J Natl Kræft
Inst 2007, 99:754�764.
119. Calle EE, Rodriguez C, Jacobs EJ, Almon ML, Chao A, McCullough ML,
Feigelson HS, Thun MJ: The American Cancer Society Cancer Prevention
Undersøgelse II Ernæringskohorte: begrundelse, undersøgelsesdesign og baseline
egenskaber. Cancer 2002, 94:2490�2501.
120. Weinstein SJ, Peters U, Ahn J, Friesen MD, Riboli E, Hayes RB, Albanes D:
Serum alfa-tocopherol og gamma-tocopherol koncentrationer og
risiko for prostatacancer i PLCO Screening Trial: en indlejret tilfældekontrol
undersøgelse. PLoS One 2012, 7:e40204.
121. Cui R, Liu ZQ, Xu Q: Blod alfa-tocopherol, gamma-tocopherol niveauer
og risiko for prostatacancer: en meta-analyse af prospektive undersøgelser.
PLoS One 2014, 9:e93044.
122. Major JM, Yu K, Weinstein SJ, Berndt SI, Hyland PL, Yeager M, Chanock S,
Albanes D: Genetiske varianter, der afspejler højere vitamin e-status hos mænd, er
forbundet med reduceret risiko for prostatacancer. J Nutr maj 2014,
144: 729 733.
123. Klein EA, Thompson IM Jr, Tangen CM, Crowley JJ, Lucia MS, Goodman PJ,
Minasian LM, Ford LG, Parnes HL, Gaziano JM, Karp DD, Lieber MM, Walther
PJ, Klotz L, Parsons JK, Chin JL, Darke AK, Lippman SM, Goodman GE,
Meyskens FL Jr, Baker LH: E-vitamin og risikoen for prostatacancer: den
Selen og E-vitamin Cancer Prevention Trial (SELECT). JAMA 2011,
306: 1549 1556.
124. Albanes D, Till C, Klein EA, Goodman PJ, Mondul AM, Weinstein SJ, aylor PR,
Parnes HL, Gaziano JM, Song X, Fleshner NE, Brown PH, Meyskens FL Jr,
Thompson IM: Plasma tocopheroler og risiko for prostatacancer i
Selen og E-vitamin Cancer Prevention Trial (SELECT). Kræft Forrige Res
(Phila) 2014, 7:886�895.
125. Kristal AR, Darke AK, Morris JS, Tangen CM, Goodman PJ, Thompson IM,
Meyskens FL Jr, Goodman GE, Minasian LM, Parnes HL, Lippman SM,
Klein EA: Baseline selenstatus og virkninger af selen og e-vitamin
tilskud på risiko for prostatacancer. J Natl Cancer Inst 2014,
106:djt456.
126. Jamison JM, Gilloteaux J, Taper HS, Summers JL: Evaluering af in vitro
og in vivo antitumoraktiviteter af vitamin C og K-3 kombinationer
mod prostatacancer hos mennesker. J Nutr 2001, 131:158S�160S.
127. Nimptsch K, Rohrmann S, Kaaks R, Linseisen J: Diætisk vitamin K-indtag
i forhold til kræftforekomst og dødelighed: resultater fra de
Heidelberg-kohorte af European Prospective Investigation in
Kræft og ernæring (EPIC-Heidelberg). Am J Clin Nutr 2010,
91: 1348 1358.
128. Ma RW, Chapman K: En systematisk gennemgang af effekten af kost i prostata
kræftforebyggelse og behandling. J Hum Nutr Diet 2009, 22:187-199.
quiz 200�182.
129. Bristow SM, Bolland MJ, MacLennan GS, Avenell A, Gray A, Gamble GD, Reid
IR: Calciumtilskud og kræftrisiko: en metaanalyse af randomiserede
kontrollerede forsøg. Br J Nutr 2013, 110:1384�1393.
130. Williams CD, Whitley BM, Hoyo C, Grant DJ, Schwartz GG, Presti JC Jr, Iraggi
JD, Newman KA, Gerber L, Taylor LA, McKeever MG, Freedland SJ: Dietary
calcium og risiko for prostatacancer: en case-kontrolundersøgelse blandt USA
veteraner. Prev Chronic Dis 2012, 9:E39.
131. Hori S, Butler E, McLoughlin J: Prostatacancer og kost: stof til eftertanke?
BJU Int 2011, 107:1348�1359.
132. Geybels MS, Verhage BA, van Schooten FJ, Goldbohm RA, van den Brandt
PA: Avanceret prostatacancerrisiko i forhold til selenniveauer i tåneglene.
J Natl Cancer Inst 2013, 105:1394�1401.
133. Singh RP, Agarwal R: Kemoforebyggelse af prostatacancer med silibinin: bænk
til sengen. Mol Carcinog 2006, 45:436-442.
134. Ting H, Deep G, Agarwal R: Molekylære mekanismer af silibinin-medieret
cancer kemoforebyggelse med stor vægt på prostatacancer.
AAPS J 2013, 15:707�716.
135. Ting HJ, Deep G, Jain AK, Cimic A, Sirintrapun J, Romero LM, Cramer SD,
Agarwal C, Agarwal R: Silibinin forhindrer prostatacancer cellemedieret
differentiering af naive fibroblaster til cancerassocierede fibroblaster
fænotype ved at målrette TGF beta2. Mol Carcinog 2014. doi:10.1002/
mc.22135. [Epub før tid]
136. Goel A, Aggarwal BB: Curcumin, det gyldne krydderi fra indisk safran, er en
kemosensibilisator og radiosensibilisator til tumorer og kemoprotector og
radiobeskytter til normale organer. Nutr Cancer 2010, 62:919�930.
137. Khan N, Adhami VM, Mukhtar H: Apoptose af diætmidler til
forebyggelse og behandling af prostatacancer. Endocr Relat Cancer 2010,
17:R39�R52.
138. Heber D: Granatæble ellagitanniner. I urtemedicin: Biomolekylær og
Kliniske aspekter. 2. udgave. Redigeret af Benzie IF, Wachtel-Galor S. Boca
Raton, FL: CRC Press; 2011.
139. Pantuck AJ, Leppert JT, Zomorodian N, Aronson W, Hong J, Barnard RJ,
Seeram N, Liker H, Wang H, Elashoff R, Heber D, Aviram M, Ignarro L,
Belldegrun A: Fase II undersøgelse af granatæblejuice til mænd med stigende
prostata-specifikt antigen efter operation eller stråling for prostata
Kræft. Clin Cancer Res 2006, 12:4018�4026.
140. Paller CJ, Ye X, Wozniak PJ, Gillespie BK, Sieber PR, Greengold RH, Stockton
BR, Hertzman BL, Efros MD, Roper RP, Liker HR, Carducci MA: En randomiseret
fase II undersøgelse af granatæbleekstrakt til mænd med stigende PSA efter
indledende behandling for lokaliseret prostatacancer. Prostatakræft Prostata Dis
2013, 16:50�55.
141. Freedland SJ, Carducci M, Kroeger N, Partin A, Rao JY, Jin Y, Kerkoutian S,
Wu H, Li Y, Creel P, Mundy K, Gurganus R, Fedor H, King SA, Zhang Y,
Heber D, Pantuck AJ: En dobbeltblind, randomiseret, neoadjuverende undersøgelse af
vævseffekterne af POMx-piller hos mænd med prostatakræft før
radikal prostatektomi. Cancer Prev Res (Phila) 2013, 6:1120�1127.
142. Wang P, Aronson WJ, Huang M, Zhang Y, Lee RP, Heber D, Henning SM:
Grøn te polyfenoler og metabolitter i prostatektomivæv:
konsekvenser for kræftforebyggelse. Cancer Prev Res (Phila) 2010,
3: 985 993.
143. Kurahashi N, Sasazuki S, Iwasaki M, Inoue M, Tsugane S: Grøn te
forbrug og risiko for prostatakræft hos japanske mænd: en prospektiv
undersøgelse. Am J Epidemiol 2008, 167:71-77.
144. McLarty J, Bigelow RL, Smith M, Elmajian D, Ankem M, Cardelli JA: Te
polyfenoler reducerer serumniveauer af prostataspecifikt antigen,
hepatocytvækstfaktor og vaskulær endotelvækstfaktor i
prostatacancerpatienter og hæmmer produktionen af hepatocytvækst
faktor og vaskulær endotelvækstfaktor in vitro. Kræft Forrige Res
(Phila) 2009, 2:673�682.
145. Bettuzzi S, Brausi M, Rizzi F, Castagnetti G, Peracchia G, Corti A:
Kemoforebyggelse af human prostatacancer ved oral administration af
grøn te-katechiner hos frivillige med højkvalitets prostata intraepitelial
neoplasi: en foreløbig rapport fra en etårig proof-of-principle undersøgelse.
Cancer Res 2006, 66:1234�1240.
146. Fraser SP, Peters A, Fleming-Jones S, Mukhey D, Djamgoz MB: Resveratrol:
hæmmende virkninger på metastatisk celleadfærd og spændingsstyret Na(+)
kanalaktivitet i rotteprostatacancer in vitro. Nutr Cancer 2014,
66: 1047 1058.
147. Oskarsson A, Spatafora C, Tringali C, Andersson AO: Inhibering af CYP17A1
aktivitet af resveratrol, piceatannol og syntetiske resveratrol-analoger.
Prostata 2014, 74:839�851.
148. Ferruelo A, Romero I, Cabrera PM, Arance I, Andres G, Angulo JC: Effekter af
resveratrol og andre vin polyphenoler på spredning, apoptose
og androgenreceptorekspression i LNCaP-celler. Actas Urol Esp Jul-Aug
2014, 38:397�404.
149. Osmond GW, Masko EM, Tyler DS, Freedland SJ, Pizzo S: In vitro og in vivo
evaluering af resveratrol og 3,5-dihydroxy-4a-acetoxy-trans-stilben i
behandling af humant prostatakarcinom og melanom. J Surg Res
2013, 179:e141�e148.
150. Baur JA, Sinclair DA: Terapeutisk potentiale af resveratrol: in vivo
beviser. Nat Rev Drug Discov 2006, 5:493�506.
151. Klink JC, Tewari AK, Masko EM, Antonelli J, Febbo PG, Cohen P, Dewhirst
MW, Pizzo SV, Freedland SJ: Resveratrol forværrer overlevelsen hos SCID-mus med prostatacancer-xenotransplantater på en cellelinjespecifik måde gennem paradoksale virkninger på onkogene veje. Prostata 2013, 73:754�762.
152. Huang EC, Zhao Y, Chen G, Baek SJ, McEntee MF, Minkin S, Biggerstaff JP,
Whelan J: Zyflamend, en polyurteblanding, nedregulerer klasse I og
klasse II histon deacetylaser og øger p21 niveauer i kastrat-resistente
prostatacancerceller. BMC Komplement Altern Med 2014, 14:68.
153. Huang EC, McEntee MF, Whelan J: Zyflamend, en kombination af urte
ekstrakter, dæmper tumorvækst i murine xenograft-modeller af
prostatakræft. Nutr Cancer 2012, 64:749�760.
154. Yan J, Xie B, Capodice JL, Katz AE: Zyflamend hæmmer udtrykket og
funktion af androgenreceptor og virker synergistisk med bicalutimid
at hæmme prostatacancer cellevækst. Prostata 2012, 72:244�252.
155. Kunnumakkara AB, Sung B, Ravindran J, Diagaradjane P, Deorukhkar A, Dey
S, Koca C, Tong Z, Gelovani JG, Guha S, Krishnan S, Aggarwal BB: Zyflamend
undertrykker vækst og sensibiliserer humane bugspytkirteltumorer til
gemcitabin i en ortotopisk musemodel gennem modulering af
flere mål. Int J Cancer 2012, 131:E292�E303.
156. Capodice JL, Gorroochurn P, Cammack AS, Eric G, McKiernan JM, Benson
MC, Stone BA, Katz AE: Zyflamend hos mænd med højkvalitets prostata
intraepitelial neoplasi: resultater af et fase I klinisk forsøg. J Soc Integr
Oncol 2009, 7:43�51.
157. Rafailov S, Cammack S, Stone BA, Katz AE: Rollen som Zyflamend, en
urte anti-inflammatorisk, som et potentielt kemoforebyggende middel mod
prostatacancer: en case-rapport. Integr Cancer Ther 2007, 6:74�76.
158. Askari F, Parizi MK, Jessri M, Rashidkhani B: Frugt- og grøntsagsindtag i
forhold til prostatacancer hos iranske mænd: en casekontrolundersøgelse.
Asian Pac J Cancer Forrige 2014, 15:5223�5227.
159. Liu B, Mao Q, Cao M, Xie L: Indtagelse af korsblomstrede grøntsager og risiko for
prostatacancer: en meta-analyse. Int J Urol 2012, 19:134�141.
160. Richman EL, Carroll PR, Chan JM: Grøntsager og frugtindtag efter
diagnose og risiko for progression af prostatacancer. Int J Cancer 2012,
131: 201 210.
161. Hsing AW, Chokkalingam AP, Gao YT, Madigan MP, Deng J, Gridley G,
Fraumeni JF Jr: Allium-grøntsager og risiko for prostatacancer: a
befolkningsbaseret undersøgelse. J Natl Cancer Inst 2002, 94:1648-1651.
162. Chan R, Lok K, Woo J: Prostatacancer og grøntsagsforbrug.
Mol Nutr Food Res 2009, 53:201�216.
163. Thomas R, Williams M, Sharma H, Chaudry A, Bellamy P: A double-blind,
placebokontrolleret randomiseret forsøg, der evaluerer effekten af en
polyphenolrig fuldkosttilskud om PSA-progression hos mænd
med prostatacancer - det britiske NCRN Pomi-T-studie. Prostatakræft Prostatakræft
Dis 2014, 17:180�186.
164. Yang CM, Lu IH, Chen HY, Hu ML: Lycopen hæmmer spredningen af
androgenafhængige humane prostatatumorceller gennem aktivering af
PPARgamma-LXRalpha-ABCA1 pathway. J Nutr Biochem 2012, 23:8-17.
165. Qiu X, Yuan Y, Vaishnav A, Tessel MA, Nonn L, van Breemen RB: Effekter af
lycopen på proteinekspression i humant primært prostataepitel
celler. Cancer Prev Res (Phila) 2013, 6:419�427.
166. Boileau TW, Liao Z, Kim S, Lemeshow S, Erdman JW Jr, Clinton SK: Prostata
carcinogenese i N-methyl-N-nitrosourea (NMU)-testosteron-behandlet
rotter fodret med tomatpulver, lycopen eller energibegrænset diæt. J Natl
Cancer Inst 2003, 95:1578�1586.
167. Konijeti R, Henning S, Moro A, Sheikh A, Elashoff D, Shapiro A, Ku M,
Said JW, Heber D, Cohen P, Aronson WJ: Chemoprevention of prostata
kræft med lycopen i TRAMP-modellen. Prostata 2010, 70:1547�1554.
168. Giovannucci E, Rimm EB, Liu Y, Stampfer MJ, Willett WC: A prospective
undersøgelse af tomatprodukter, lycopen og risiko for prostatakræft. J Natl
Cancer Inst 2002, 94:391�398.
169. Zu K, Mucci L, Rosner BA, Clinton SK, Loda M, Stampfer MJ, Giovannucci E:
Diætlycopen, angiogenese og prostatacancer: en prospektiv
undersøgelse i den prostata-specifikke antigen-æra. J Natl Cancer Inst 2014,
106:djt430.
170. Gann PH, Ma J, Giovannucci E, Willett W, Sacks FM, Hennekens CH, Stampfer
MJ: Lavere risiko for prostatacancer hos mænd med forhøjet plasmalycopen
niveauer: resultater af en prospektiv analyse. Cancer Res 1999, 59:1225-1230.
171. Kristal AR, Till C, Platz EA, Song X, King IB, Neuhouser ML, Ambrosone CB,
Thompson IM: Serumlycopenkoncentration og risiko for prostatacancer:
resultater fra forsøget med forebyggelse af prostatakræft. Kræftepidemiol
Biomarkører Prev 2011, 20:638�646.
172. Kirsh VA, Mayne ST, Peters U, Chatterjee N, Leitzmann MF, Dixon LB, Urban
DA, Crawford ED, Hayes RB: En prospektiv undersøgelse af lycopen og tomat
produktindtag og risiko for prostatacancer. Cancer Epidemiol Biomarkører
Forrige 2006, 15:92�98.
173. Mariani S, Lionetto L, Cavallari M, Tubaro A, Rasio D, De Nunzio C, Hong
GM, Borro M, Simmaco M: Lav prostatakoncentration af lycopen er
forbundet med udvikling af prostatacancer hos patienter med høj grad
prostatisk intraepitelial neoplasi. Int J Mol Sci 2014, 15:1433-1440.
174. Kucuk O, Sarkar FH, Djuric Z, Sakr W, Pollak MN, Khachik F, Banerjee M,
Bertram JS, Wood DP Jr: Effekter af lycopentilskud hos patienter
med lokaliseret prostatacancer. Exp Biol Med (Maywood) 2002, 227:881�885.
175. Chen L, Stacewicz-Sapuntzakis M, Duncan C, Sharifi R, Ghosh L, van
Breemen R, Ashton D, Bowen PE: Oxidativ DNA-skade i prostata
kræftpatienter, der indtager tomatsauce-baserede hovedretter som helføde
intervention. J Natl Cancer Inst 2001, 93:1872-1879.
176. van Breemen RB, Sharifi R, Viana M, Pajkovic N, Zhu D, Yuan L, Yang Y,
Bowen PE, Stacewicz-Sapuntzakis M: Antioxidantvirkninger af lycopen i
Afroamerikanske mænd med prostatacancer eller benign prostatahyperplasi:
et randomiseret, kontrolleret forsøg. Cancer Prev Res (Phila) 2011, 4:711�718.
177. Shafique K, McLoone P, Qureshi K, Leung H, Hart C, Morrison DS: Kaffe
forbrug og risiko for prostatacancer: yderligere bevis for omvendt
forhold. Nutr J 2012, 11:42.
178. Wilson KM, Kasperzyk JL, Rider JR, Kenfield S, van Dam RM, Stampfer MJ,
Giovannucci E, Mucci LA: Kaffeforbrug og risiko for prostatakræft
og progression i Health Professionals Follow-up Study. J Natl
Cancer Inst 2011, 103:876�884.
179. Bosire C, Stampfer MJ, Subar AF, Wilson KM, Park Y, Sinha R: Coffee
forbrug og risikoen for generel og dødelig prostatakræft i
NIH-AARP kost- og sundhedsundersøgelse. Cancer Causes Control 2013, 24:1527�1534.
180. Arab L, Su LJ, Steck SE, Ang A, Fontham ET, Bensen JT, Mohler JL: Kaffe
forbrug og prostatacancer aggressivitet blandt afrikanske og
Kaukasiske amerikanere i en befolkningsbaseret undersøgelse. Nutr Cancer 2012,
64: 637 642.
181. Phillips RL, Snowdon DA: Association of meat and coffee use with cancers
af tyktarmen, brystet og prostata blandt syvendedags adventister:
foreløbige resultater. Cancer Res 1983, 43:2403 s�2408s.
182. Hsing AW, McLaughlin JK, Schuman LM, Bjelke E, Gridley G, Wacholder S,
Chien HT, Blot WJ: Diæt, tobaksbrug og dødelig prostatakræft: resultater
fra det lutherske broderskabs kohortestudie. Cancer Res 1990,
50: 6836 6840.
183. Cao S, Liu L, Yin X, Wang Y, Liu J, Lu Z: Kaffeforbrug og risiko for
prostatacancer: en meta-analyse af prospektive kohortestudier.
Carcinogenese 2014, 35:256�261.
184. Nordmann AJ, Suter-Zimmermann K, Bucher HC, Shai I, Tuttle KR,
Estruch R, Briel M: Meta-analyse, der sammenligner Middelhavet med fedtfattigt
diæter til modifikation af kardiovaskulære risikofaktorer. Am J Med 2011,
124:841�851. e842.
185. Kapiszewska M: Et forhold mellem grøntsager og kødforbrug som relevant
faktor, der bestemmer kræftforebyggende kost. Middelhavet kontra
andre europæiske lande. Forum Nutr 2006, 59:130�153.
186. Kenfield SA, Dupre N, Richman EL, Stampfer MJ, Chan JM, Giovannucci EL:
Middelhavskost og risiko for prostatacancer og dødelighed i sundhed
Professionelle opfølgningsundersøgelse. Eur Urol 2014, 65:887�894.
187. Ambrosini GL, Fritschi L, de Klerk NH, Mackerras D, Leavy J: Kostmønstre
identificeret ved hjælp af faktoranalyse og prostatacancerrisiko: en sagskontrol
studere i det vestlige Australien. Ann Epidemiol 2008, 18:364–370.
188. Baade PD, Youlden DR, Krnjacki LJ: International epidemiology of prostata
kræft: geografisk fordeling og sekulære tendenser. Mol Nutr Food Res
2009, 53:171�184.
189. Muller DC, Severi G, Baglietto L, Krishnan K, engelsk DR, Hopper JL, Giles GG:
Kostmønstre og risiko for prostatakræft. Cancer Epidemiol Biomarkers Prev
2009, 18:3126�3129.
190. Tseng M, Breslow RA, DeVellis RF, Ziegler RG: Kostmønstre og prostata
kræftrisiko i den nationale sundheds- og ernæringsundersøgelse
Epidemiologisk opfølgningsstudiekohorte. Cancer Epidemiol Biomarkers Prev
2004, 13:71�77.
191. Wu K, Hu FB, Willett WC, Giovannucci E: Kostmønstre og risiko for
prostatakræft hos amerikanske mænd. Cancer Epidemiol Biomarkers Prev 2006,
15: 167 171.
192. Daubenmier JJ, Weidner G, Marlin R, Crutchfield L, Dunn-Emke S, Chi C,
Gao B, Carroll P, Ornish D: Livsstil og sundhedsrelateret livskvalitet
mænd med prostatakræft klares med aktiv overvågning. Urologi
2006, 67:125�130.
193. Parsons JK, Newman VA, Mohler JL, Pierce JP, Flatt S, Marshall J: Dietary
modifikation hos patienter med prostatacancer ved aktiv overvågning: a
randomiseret, multicenter forundersøgelse. BJU Int 2008, 101:1227�1231.
194. Mosher CE, Sloane R, Morey MC, Snyder DC, Cohen HJ, Miller PE,
Demark-Wahnefried W: Sammenhæng mellem livsstilsfaktorer og kvalitet
af livet blandt ældre langvarig bryst-, prostata- og tyktarmskræft
overlevende. Cancer 2009, 115:4001�4009.
195. Bhindi B, Locke J, Alibhai SM, Kulkarni GS, Margel DS, Hamilton RJ, Finelli A,
Trachtenberg J, Zlotta AR, Toi A, Hersey KM, Evans A, van der Kwast TH,
Fleshner NE: Dissekere sammenhængen mellem metabolisk syndrom
og prostatacancerrisiko: analyse af en stor klinisk kohorte. Eur Urol 2014.
doi:10.1016/j.eururo.2014.01.040. [Epub før tid]
196. Esposito K, Chiodini P, Capuano A, Bellastella G, Maiorino MI, Parretta E,
Lenzi A, Giugliano D: Virkning af metabolisk syndrom og dets komponenter
om risiko for prostatacancer: meta-analyse. J Endocrinol Invest 2013,
36: 132 139.
197. US Department of Agriculture og US Department of Health and
Menneskelige tjenester. Dietary Guidelines for Americans, 2010. 7. udgave.
Washington, DC: US Government Printing Office, december 2010.
Luk harmonika
Oplysningerne heri om "Prostatakræft, ernæring og diætinterventioner" er ikke beregnet til at erstatte et en-til-en-forhold med en kvalificeret sundhedsperson eller autoriseret læge og er ikke medicinsk rådgivning. Vi opfordrer dig til at træffe sundhedsbeslutninger baseret på din forskning og partnerskab med en kvalificeret sundhedsperson.
Bloginformation og diskussioner om omfang
Vores informationsomfang er begrænset til kiropraktik, muskuloskeletal, fysisk medicin, wellness, bidragende ætiologisk viscerosomatiske forstyrrelser inden for kliniske præsentationer, tilhørende somatovisceral refleks klinisk dynamik, subluksationskomplekser, følsomme helbredsproblemer og/eller funktionel medicin artikler, emner og diskussioner.
Vi giver og præsenterer klinisk samarbejde med specialister fra forskellige discipliner. Hver specialist er styret af deres faglige omfang af praksis og deres licensjurisdiktion. Vi bruger funktionelle sundheds- og velværeprotokoller til at behandle og understøtte pleje af skader eller lidelser i bevægeapparatet.
Vores videoer, indlæg, emner, emner og indsigt dækker kliniske forhold, problemstillinger og emner, der relaterer til og direkte eller indirekte understøtter vores kliniske anvendelsesområde.*
Vores kontor har med rimelighed forsøgt at give støttende citater og har identificeret den eller de relevante forskningsundersøgelser, der understøtter vores indlæg. Vi leverer kopier af understøttende forskningsundersøgelser tilgængelige for tilsynsråd og offentligheden efter anmodning.
Vi forstår, at vi dækker forhold, der kræver yderligere forklaring på, hvordan det kan hjælpe med en bestemt plejeplan eller behandlingsprotokol. derfor er du velkommen til at spørge for yderligere at diskutere emnet ovenfor Dr. Alex Jimenez, DC, eller kontakte os på 915-850-0900.
Vi er her for at hjælpe dig og din familie.
Blessings
Dr. Alex Jimenez A.D. MSACP, RN*, CCST, Ifmcp*, CIFM*, ATN*
Email: coach@elpasofunctionalmedicine.com
Licenseret som Doctor of Chiropractic (DC) i Texas & New Mexico*
Texas DC-licensnummer TX5807, New Mexico DC Licensnr. NM-DC2182
Licenseret som registreret sygeplejerske (RN*) in Florida
Florida-licens RN-licens # RN9617241 (Kontrol nr. 3558029)
Kompakt status: Multi-State Licens: Bemyndiget til at praktisere i 40 stater*
Dr. Alex Jimenez DC, MSACP, RN*CIFM*, IFMCP*, ATN*, CCST
Mit digitale visitkort






