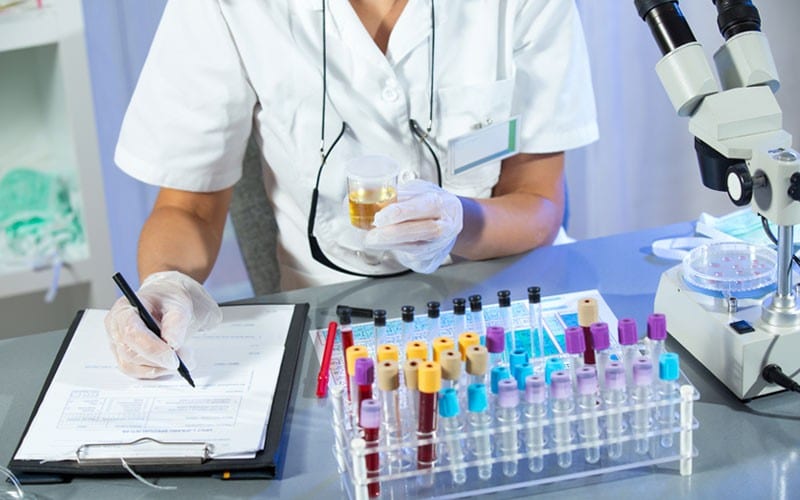
Depression er et af de mest almindelige psykiske problemer i USA. Aktuel forskning tyder på, at depression skyldes en kombination af genetiske, biologiske, økologiske og psykologiske aspekter. Depression er en alvorlig psykiatrisk lidelse verden over med en betydelig økonomisk og psykologisk belastning for samfundet. Heldigvis kan depression, selv de mest alvorlige tilfælde, behandles. Jo tidligere behandlingen kan begynde, jo mere effektiv er den.
Som et resultat er der dog et behov for robuste biomarkører, som vil hjælpe med at forbedre diagnosen for at fremskynde lægemiddel- og/eller medicinopdagelsesprocessen for hver patient med lidelsen. Disse er objektive, perifere fysiologiske indikatorer, hvis tilstedeværelse kan bruges til at forudsige sandsynligheden for indtræden eller eksistensen af depression, stratificere i henhold til sværhedsgrad eller symptomatologi, indikere forudsigelse og prognose eller overvåge respons på terapeutiske indgreb. Formålet med den følgende artikel er at demonstrere nyere indsigt, aktuelle udfordringer og fremtidsudsigter vedrørende opdagelsen af en række forskellige biomarkører for depression og hvordan disse kan hjælpe med at forbedre diagnosticering og behandling.
Indhold
Biomarkører for depression: Nylig indsigt, aktuelle udfordringer og fremtidsudsigter
Abstrakt
Et væld af forskning har impliceret hundredvis af formodede biomarkører for depression, men har endnu ikke fuldt ud klarlagt deres roller i depressiv sygdom eller fastslået, hvad der er unormalt hos hvilke patienter, og hvordan biologisk information kan bruges til at forbedre diagnose, behandling og prognose. Denne mangel på fremskridt skyldes delvist depressionens natur og heterogenitet, sammenholdt med metodologisk heterogenitet inden for forskningslitteraturen og den store vifte af biomarkører med potentiale, hvis udtryk ofte varierer afhængigt af mange faktorer. Vi gennemgår den tilgængelige litteratur, som indikerer, at markører involveret i inflammatoriske, neurotrofiske og metaboliske processer, såvel som neurotransmitter og neuroendokrine systemkomponenter, repræsenterer meget lovende kandidater. Disse kan måles gennem genetiske og epigenetiske, transkriptomiske og proteomiske, metabolomiske og neuroimaging vurderinger. Brugen af nye tilgange og systematiske forskningsprogrammer er nu påkrævet for at bestemme, om og hvilke biomarkører der kan bruges til at forudsige respons på behandling, stratificere patienter til specifikke behandlinger og udvikle mål for nye interventioner. Vi konkluderer, at der er meget løfte om at reducere byrden af depression gennem yderligere udvikling og udvidelse af disse forskningsmuligheder.
nøgleord: humørlidelse, svær depressiv lidelse, inflammation, behandlingsrespons, lagdeling, personlig medicin
Introduktion
Udfordringer i mental sundhed og humørforstyrrelser
Selvom psykiatrien har en sygdomsrelateret byrde, der er større end nogen anden medicinsk diagnostisk kategori,1 er en forskel i agtelse stadig tydelig mellem fysisk og mental sundhed på tværs af mange områder, herunder forskningsfinansiering2 og publikation.3 Blandt de vanskeligheder, som mental sundhed står over for, er mangel af konsensus omkring klassificering, diagnose og behandling, der udspringer af en ufuldstændig forståelse af de processer, der ligger til grund for disse lidelser. Dette er meget tydeligt i humørsygdomme, den kategori, der udgør den største enkeltbyrde i mental sundhed.3 Den mest udbredte stemningslidelse, major depressive disorder (MDD), er en kompleks, heterogen sygdom, hvor op til 60 % af patienterne kan opleve en vis grad af behandlingsresistens, der forlænger og forværrer episoder.4 For humørsygdomme og i det bredere felt af mental sundhed vil behandlingsresultater sandsynligvis blive forbedret ved opdagelsen af robuste, homogene undertyper inden for (og på tværs af) diagnostiske kategorier, hvorved behandlinger kunne stratificeres. I erkendelse af dette er globale initiativer til at afgrænse funktionelle undertyper nu i gang, såsom forskningsdomænekriterierne.5 Det er blevet hævdet, at biologiske markører er prioriterede kandidater til at undertypebestemme psykiske lidelser.6
Forbedring af respons på behandlinger for depression
På trods af en lang række behandlingsmuligheder for svær depression opnår kun cirka en tredjedel af patienter med MDD remission, selv når de modtager optimal antidepressiv behandling i henhold til konsensusretningslinjer og ved brug af målebaseret pleje, og frekvensen af behandlingsrespons ser ud til at falde med hver ny behandling .7 Ydermere er behandlingsresistent depression (TRD) forbundet med øget funktionsnedsættelse, mortalitet, sygelighed og tilbagevendende eller kroniske episoder på lang sigt.8,9 At opnå forbedringer i behandlingsrespons på ethvert klinisk stadie ville således give bredere fordele for overordnede resultater ved depression. På trods af den betydelige byrde, der kan tilskrives TRD, har forskningen på dette område været sparsom. Definitioner af TRD er ikke standardiserede på trods af tidligere forsøg:4 nogle kriterier kræver kun ét behandlingsforsøg, der ikke opnår en 50 % symptomscorereduktion (fra et valideret mål for depressions sværhedsgrad), mens andre kræver manglende opnåelse af fuld remission eller manglende respons på mindst to tilstrækkeligt afprøvede antidepressiva af forskellige klasser inden for en episode for at blive betragtet som TRD.4,10 Ydermere forbedres stadieinddelingen og forudsigelsen af behandlingsresistens ved at føje de centrale kliniske karakteristika for sværhedsgrad og kronicitet til antallet af mislykkede behandlinger .9,11 Ikke desto mindre gør denne inkonsistens i definitionen fortolkningen af forskningslitteraturen om TRD til en endnu mere kompleks opgave.
For at forbedre respons på behandlinger er det klart nyttigt at identificere forudsigelige risikofaktorer for manglende respons. Nogle generelle prædiktorer for TRD er blevet karakteriseret, herunder mangel på fuld remission efter tidligere episoder, komorbid angst, suicidalitet og tidlig indtræden af depression, såvel som personlighed (især lav ekstraversion, lav belønningsafhængighed og høj neuroticisme) og genetiske faktorer.12 Disse resultater bekræftes af anmeldelser, der syntetiserer evidensen separat for farmakologisk13 og psykologisk14 behandling af depression. Antidepressiva og kognitive adfærdsterapier viser omtrent sammenlignelig effekt15, men på grund af deres forskellige virkningsmekanismer kan det forventes at have forskellige prædiktorer for respons. Mens traumer i det tidlige liv længe har været forbundet med dårligere kliniske resultater og reduceret respons på behandling,16 tyder tidlige indikationer på, at mennesker med en historie med barndomstraumer kan reagere bedre på psykologiske end farmakologiske behandlinger.17 På trods af dette hersker der usikkerhed og ringe personalisering eller stratificering af behandlingen har nået klinisk praksis.18
Denne gennemgang fokuserer på evidensen, der understøtter brugen af biomarkører som potentielt nyttige kliniske værktøjer til at forbedre behandlingsresponsen for depression.
Biomarkører: systemer og kilder
Biomarkører udgør et potentielt mål for at identificere prædiktorer for respons på forskellige indgreb.19 De hidtidige beviser tyder på, at markører, der afspejler aktiviteten af inflammatoriske, neurotransmitter-, neurotrofiske, neuroendokrine og metaboliske systemer, kan være i stand til at forudsige mentale og fysiske helbredsudfald hos aktuelt deprimerede individer , men der er meget uoverensstemmelse mellem resultaterne.20 I denne gennemgang fokuserer vi på disse fem biologiske systemer.
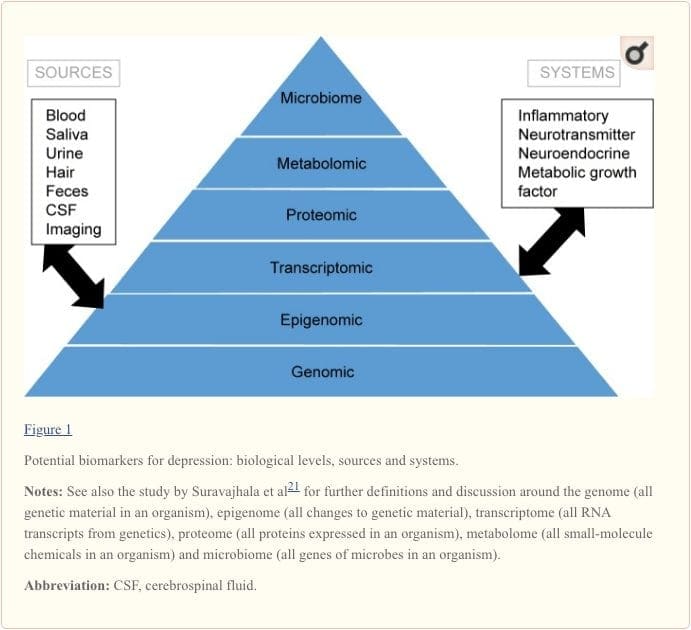
For at opnå en fuld forståelse af molekylære veje og deres bidrag til psykiatriske lidelser, anses det nu for vigtigt at vurdere flere biologiske niveauer, i det, der populært omtales som en �omics� tilgang.21 Figur 1 giver en skildring af de forskellige biologiske niveauer, hvor hvert af de fem systemer kan vurderes, og de potentielle kilder til markører, som disse vurderinger kan foretages på. Bemærk dog, at mens hvert system kan inspiceres på hvert omics-niveau, varierer de optimale målekilder klart på hvert niveau. For eksempel giver neuroimaging en platform for indirekte vurdering af hjernens struktur eller funktion, mens proteinundersøgelser i blod direkte vurderer markører. Transcriptomics22 og metabolomics23 er stadig mere populære og tilbyder vurdering af potentielt enorme antal markører, og Human Microbiome Project forsøger nu at identificere alle mikroorganismer og deres genetiske sammensætning i mennesker.24 Nye teknologier forbedrer vores evne til at måle disse, herunder gennem yderligere kilder ; for eksempel kan hormoner som kortisol nu analyseres i hår eller fingernegle (som giver en kronisk indikation) eller sved (ved kontinuerlig måling)25 såvel som i blod, cerebrospinalvæske, urin og spyt.
I betragtning af antallet af formodede kilder, niveauer og systemer involveret i depression, er det ikke overraskende, at omfanget af biomarkører med translationspotentiale er omfattende. Især når interaktioner mellem markører overvejes, er det måske usandsynligt, at undersøgelse af enkelte biomarkører isoleret vil give resultater, der er frugtbare for at forbedre klinisk praksis. Schmidt et al26 foreslog brugen af biomarkørpaneler, og efterfølgende skitserede Brand et al27 et udkast til panel baseret på tidligere klinisk og præklinisk evidens for MDD, der identificerede 16 �stærke� biomarkørmål, som hver især sjældent er en enkelt markør. De omfatter reduceret gråstofvolumen (i hippocampale, præfrontale cortex og basale ganglier), circadian cyklusændringer, hypercortisolisme og andre repræsentationer af hyperaktivering af hypothalamus-hypofyse-binyreaksen (HPA), skjoldbruskkirteldysfunktion, reduceret dopamin, noradrenalin eller 5-hydroxyindol , øget glutamat, øget superoxiddismutase og lipidperoxidation, svækket cyklisk adenosin 3a,5a-monophosphat og mitogen-aktiveret proteinkinase pathway aktivitet, øgede proinflammatoriske cytokiner, ændringer til tryptophan, kynurenin, insulin og specifikke genetiske polymorfismer. Disse markører er ikke blevet vedtaget ved konsensus og kunne måles på forskellige måder; det er klart, at fokuseret og systematisk arbejde skal løse denne enorme opgave for at bevise deres kliniske fordele.
Formålet med denne anmeldelse
Som en bevidst bred gennemgang søger denne artikel at bestemme de overordnede behov for biomarkørforskning i depression og i hvilken udstrækning biomarkører har et reelt translationelt potentiale for at forbedre respons på behandlinger. Vi begynder med at diskutere de vigtigste og mest spændende resultater på dette felt og leder læseren til mere specifikke anmeldelser vedrørende relevante markører og sammenligninger. Vi skitserer de aktuelle udfordringer i lyset af beviserne, i kombination med behov for at reducere byrden af depression. Endelig ser vi frem til de vigtige forskningsveje til at imødegå aktuelle udfordringer og deres implikationer for klinisk praksis.
Seneste indsigt
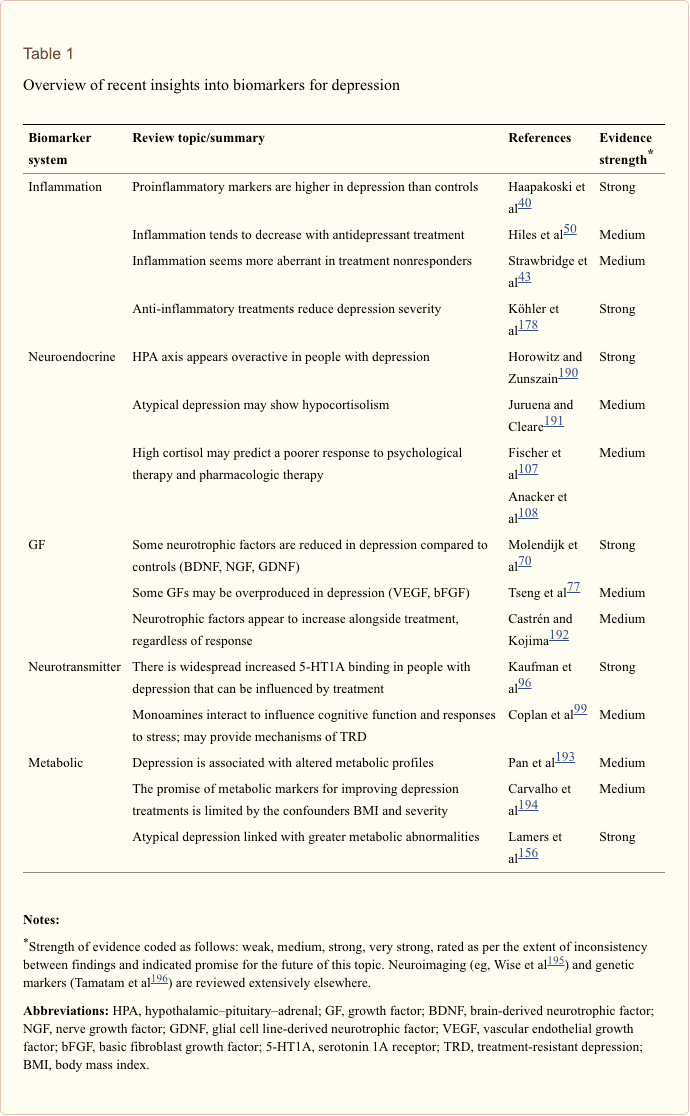
Søgningen efter klinisk nyttige biomarkører for mennesker med depression har genereret omfattende undersøgelser i løbet af det sidste halve århundrede. De mest almindeligt anvendte behandlinger blev udtænkt fra monoaminteorien om depression; efterfølgende fik neuroendokrine hypoteser stor opmærksomhed. I de senere år har den mest produktive forskning omgivet den inflammatoriske hypotese om depression. En lang række relevante oversigtsartikler har dog fokuseret på alle fem systemer; se tabel 1 og nedenfor for en samling af nyere indsigter på tværs af biomarkørsystemer. Mens de er målt på mange niveauer, er blodafledte proteiner blevet undersøgt mest udbredt og giver en kilde til biomarkør, der er bekvem, omkostningseffektiv og kan være tættere på translationspotentiale end andre kilder; således gives flere detaljer til biomarkører, der cirkulerer i blodet.
I en nylig systematisk gennemgang undersøgte Jani et al20 perifere blod-baserede biomarkører for depression i forbindelse med behandlingsresultater. Ud af kun 14 inkluderede undersøgelser (søgt frem til begyndelsen af 2013) blev 36 biomarkører undersøgt, hvoraf 12 var signifikante forudsigere for mentale eller fysiske responsindekser i mindst én undersøgelse. De identificerede som potentielt repræsenterende risikofaktorer for manglende respons inkluderede inflammatoriske proteiner: lavt interleukin (IL)-12p70, forholdet mellem lymfocyt- og monocytantal; neuroendokrine markører (dexamethason ikke-suppression af cortisol, højt cirkulerende kortisol, reduceret thyreoidea-stimulerende hormon); neurotransmittermarkører (lavt serotonin og noradrenalin); metaboliske (low high-density lipoprotein cholesterol) og neurotrofiske faktorer (reduceret S100 calciumbindende protein B). Ud over dette har andre anmeldelser rapporteret om sammenhænge mellem yderligere biomarkører og behandlingsresultater.19,28�30 En kort beskrivelse af formodede markører i hvert system er skitseret i de efterfølgende afsnit og i tabel 2.
Inflammatoriske fund ved depression
Siden Smiths banebrydende papir, der skitserer makrofaghypotesen31, har denne etablerede litteratur fundet øgede niveauer af forskellige proinflammatoriske markører hos deprimerede patienter, som er blevet gennemgået bredt.32�37 Tolv inflammatoriske proteiner er blevet evalueret i metaanalyser, der sammenligner deprimerede og raske kontrolpopulationer.38�43
IL-6 (P<0.001 i alle metaanalyser; 31 undersøgelser inkluderet) og CRP (P<0.001; 20 undersøgelser) forekommer hyppigt og pålideligt forhøjet ved depression.40 Forhøjet tumornekrosefaktor alfa (TNF?) blev identificeret i tidlige undersøgelser (P<0.001),38, men væsentlig heterogenitet gjorde dette inkonklusivt, når der tages højde for nyere undersøgelser (31 undersøgelser).40 IL-1? er endnu mere uendeligt forbundet med depression, med metaanalyser, der tyder på højere niveauer af depression (P=0.03),41 høje niveauer kun i europæiske undersøgelser42 eller ingen forskelle fra kontroller.40 På trods af dette foreslog en nylig artikel særlige translationelle implikationer for IL- 1a,44 understøttet af en ekstremt signifikant effekt af forhøjet IL-1? ribonukleinsyre, der forudsiger et dårligt respons på antidepressiva;45 andre fund ovenfor vedrører cirkulerende blod-afledte cytokiner. Kemokinmonocyt kemoattraktant protein-1 har vist forhøjelser hos deprimerede deltagere i en meta-analyse.39 Interleukiner IL-2, IL-4, IL-8, IL-10 og interferon gamma var ikke signifikant forskellige mellem deprimerede patienter og kontroller ved en meta-analytisk niveau, men har ikke desto mindre vist potentiale i forhold til at ændre med behandling: IL-8 er blevet rapporteret som forhøjet hos dem med svær depression prospektivt og tværsnitsmæssigt, 46 forskellige mønstre for forandring i IL-10 og interferon gamma under behandling er forekommet mellem tidlige respondere versus non-responders,47 mens IL-4 og IL-2 er faldet i takt med symptomremission.48 I metaanalyser er små fald sideløbende med behandling blevet påvist for IL-6, IL-1?, IL- 10 og CRP.43,49,50 Derudover TNF? kan kun reduceres med behandling hos respondere, og et sammensat markørindeks kan indikere øget inflammation hos patienter, som efterfølgende ikke reagerer på behandlingen.43 Det er dog bemærkelsesværdigt, at næsten al forskning, der undersøger inflammatoriske proteiner og behandlingsrespons, anvender farmakologiske behandlingsforsøg. . Således kan i det mindste nogle inflammatoriske ændringer under behandlingen sandsynligvis tilskrives antidepressiva. De præcise inflammatoriske virkninger af forskellige antidepressiva er endnu ikke fastlagt, men beviser, der anvender CRP-niveauer, tyder på, at individer reagerer forskelligt på specifikke behandlinger baseret på baseline-inflammation: Harley et al51 rapporterede forhøjet CRP før behandling, der forudsiger en dårlig respons på psykologisk terapi (kognitiv adfærd eller interpersonel). psykoterapi), men en god respons på nortriptylin eller fluoxetin; Uher et al52 gentog dette fund for nortriptylin og identificerede den modsatte effekt for escitalopram. I modsætning hertil fandt Chang et al53 højere CRP hos tidlige respondere på fluoxetin eller venlafaxin end non-responders. Desuden har patienter med TRD og høj CRP reageret bedre på TNF? antagonist infliximab end dem med niveauer i normalområdet.54
Tilsammen tyder evidensen på, at selv når der kontrolleres for faktorer som kropsmasseindeks (BMI) og alder, forekommer inflammatoriske reaktioner afvigende hos cirka en tredjedel af patienter med depression.55,56. Det inflammatoriske system er imidlertid ekstremt komplekst, og der er talrige biomarkører, der repræsenterer forskellige aspekter af dette system. For nylig har yderligere nye cytokiner og kemokiner givet tegn på abnormiteter i depression. Disse omfatter: makrofaghæmmende protein 1a, IL-1a, IL-7, IL-12p70, IL-13, IL-15, eotaxin, granulocyt makrofag kolonistimulerende faktor,57 IL-5,58 IL-16,59 IL- 17,60 monocyt kemoattraktant protein-4,61 thymus og aktiveringsreguleret kemokin,62 eotaxin-3, TNFb,63 interferon gamma-induceret protein 10,64 serum amyloid A,65 opløseligt intracellulært adhæsionsmolekyle66 og opløseligt molekyle 1.67 vaskulær celle og opløselig XNUMX vaskulær celle
Vækstfaktorfund i depression
I lyset af den potentielle betydning af ikke-neurotrofiske vækstfaktorer (såsom dem, der vedrører angiogenese), henviser vi til neurogene biomarkører under den bredere definition af vækstfaktorer.
Hjerneafledt neurotrofisk faktor (BDNF) er den hyppigst undersøgte af disse. Flere meta-analyser viser svækkelse af BDNF-proteinet i serum, som ser ud til at stige sideløbende med antidepressiv behandling.68�71 Den seneste af disse analyser tyder på, at disse BDNF-afvigelser er mere udtalte hos de mest alvorligt deprimerede patienter, men at antidepressiva ser ud til at øge niveauerne af dette protein selv i fravær af klinisk remission.70 proBDNF er blevet mindre bredt undersøgt end den modne form af BDNF, men de to ser ud til at adskille sig funktionelt (med hensyn til deres virkninger på tyrosinreceptorkinase B-receptorer) og nylige beviser tyder på, at mens moden BDNF kan reduceres ved depression, kan proBDNF være overproduceret.72 Nervevækstfaktor vurderet perifert er også blevet rapporteret som lavere ved depression end hos kontroller i en meta-analyse, men kan muligvis ikke ændres af antidepressiv behandling på trods af at mest svækket hos patienter med mere alvorlig depression.73 Lignende fund er blevet rapporteret i en metaanalyse for gliacellerlinjeafledt neurotrofisk faktor.74
Vaskulær endotelvækstfaktor (VEGF) spiller en rolle i at fremme angiogenese og neurogenese sammen med andre medlemmer af VEGF-familien (f.eks. VEGF-C, VEGF-D) og har løfte om depression.75 På trods af inkonsekvente beviser har to metaanalyser for nylig indikerede forhøjelser af VEGF i blod fra deprimerede patienter sammenlignet med kontroller (på tværs af 16 undersøgelser; P<0.001).76,77 Lavt VEGF er imidlertid blevet identificeret i TRD78, og højere niveauer har forudsagt manglende respons på antidepressiv behandling.79 Det er ikke forstået hvorfor niveauet af VEGF-protein ville være forhøjet, men det kan til dels tilskrives proinflammatorisk aktivitet og/eller stigninger i blod-hjernebarriere-permeabilitet i deprimerede tilstande, der forårsager nedsat ekspression i cerebrospinalvæske.80 Forholdet mellem VEGF og behandlingsrespons er uklart. ; en nylig undersøgelse fandt ingen sammenhæng mellem hverken serum VEGF eller BDNF med respons eller depressions sværhedsgrad, på trods af fald sammen med antidepressiv behandling.81 Insulinlignende vækstfaktor-1 er en yderligere faktor med neurogene funktioner, der kan øges ved depression, hvilket afspejler en ubalance i neurotrofiske processer.82,83 Grundlæggende fibroblastvækstfaktor (eller FGF-2) er medlem af fibroblastvækstfaktorfamilien og forekommer højere i deprimerede end kontrolgrupper.84 Rapporter er dog ikke konsistente; man fandt, at dette protein var lavere i MDD end raske kontroller, men reducerede yderligere sammen med antidepressiv behandling.85
Yderligere vækstfaktorer, der ikke er blevet tilstrækkeligt undersøgt i depression, omfatter tyrosinkinase 2 og opløselig fms-lignende tyrosinkinase-1 (også kaldet sVEGFR-1), som virker i synergi med VEGF, og tyrosinkinasereceptorer (der binder BDNF) kan svækkes i depression.86 Placental vækstfaktor er også en del af VEGF-familien, men er ikke blevet undersøgt i systematisk deprimerede prøver, så vidt vi ved.
Metaboliske biomarkørfund i depression
De vigtigste biomarkører forbundet med metabolisk sygdom omfatter leptin, adiponectin, ghrelin, triglycerider, high-density lipoprotein (HDL), glucose, insulin og albumin.87 Forbindelserne mellem mange af disse og depression er blevet gennemgået: leptin88 og ghrelin89 forekommer lavere ved depression. end kontroller i periferien og kan stige sammen med antidepressiv behandling eller remission. Insulinresistens kan være øget ved depression, omend med små mængder.90 Lipidprofiler, inklusive HDL-kolesterol, ser ud til at være ændret hos mange patienter med depression, inklusive dem uden komorbid fysisk sygdom, selvom dette forhold er komplekst og kræver yderligere belysning.91 Derudover, hyperglykæmi92 og hypoalbuminæmi93 ved depression er blevet rapporteret i anmeldelser.
Undersøgelser af overordnede metaboliske tilstande bliver hyppigere ved at bruge metabolomiske paneler af små molekyler med håbet om at finde en robust biokemisk signatur for psykiatriske lidelser. I et nyligt studie, der anvender kunstig intelligens-modellering, var et sæt metabolitter, der illustrerer øget glucose-lipid-signalering, meget forudsigende for en MDD-diagnose94, der understøttede tidligere undersøgelser.95
Neurotransmitterfund ved depression
Mens opmærksomheden på monoaminer i depression har givet relativt vellykkede behandlinger, er der ikke identificeret robuste neurotransmittermarkører for at optimere behandlingen baseret på selektiviteten af monoamin-mål for antidepressiva. Nyligt arbejde peger på, at serotonin (5-hydroxytryptamin) 1A-receptoren er potentielt vigtig for både diagnose og prognose af depression, i afventning af nye genetiske og billeddiagnostiske teknikker.96 Der er nye potentielle behandlinger rettet mod 5-hydroxytryptamin; for eksempel ved brug af en administration af 5-hydroxytryptophan med langsom frigivelse.97 Øget transmission af dopamin interagerer med andre neurotransmittere for at forbedre kognitive resultater såsom beslutningstagning og motivation.98 På samme måde kan neurotransmitterne glutamat, noradrenalin, histamin og serotonin interagere og aktiveres som en del af en depressionsrelateret stressreaktion; dette kan reducere produktionen af 5-hydroxytryptamin gennem oversvømmelser . En nylig gennemgang opstiller denne teori og foreslår, at i TRD kan dette vendes (og 5-HT genoprettes) gennem multimodal behandling rettet mod flere neurotransmittere.99 Interessant nok forekommer stigninger i serotonin ikke altid sammen med terapeutiske antidepressive fordele.100 På trods af dette , neurotransmittermetabolitter såsom 3-methoxy-4-hydroxyphenylglycol, af noradrenalin eller homovanillinsyre, af dopamin, har ofte vist sig at stige sammen med reduktion af depression med antidepressiv behandling101,102 eller at lave niveauer af disse metabolitter forudsiger en bedre respons på SSRI-behandling.102,103
Neuroendokrine fund ved depression
Cortisol er den mest almindelige HPA-akse biomarkør, der er blevet undersøgt ved depression. Talrige anmeldelser har fokuseret på de forskellige vurderinger af HPA-aktivitet; samlet set tyder disse på, at depression er forbundet med hypercortisolæmi, og at cortisol-opvågningsreaktionen ofte er svækket.104,105 Dette understøttes af en nylig gennemgang af kroniske cortisolniveauer målt i hår, hvilket understøtter hypotesen om cortisolhyperaktivitet ved depression, men hypoaktivitet ved andre sygdomme som f.eks. som panikangst.106 Ydermere kan især forhøjede cortisolniveauer forudsige en dårligere respons på psykologisk107 og antidepressiv108 behandling. Historisk set har den mest lovende neuroendokrine markør for prospektiv behandlingsrespons været dexamethason-suppressionstesten, hvor cortisol-non-suppression efter dexamethasonadministration er forbundet med en lavere sandsynlighed for efterfølgende remission. Dette fænomen er dog ikke blevet betragtet som tilstrækkelig robust til klinisk anvendelse. Beslægtede markører corticotrophin-releasing hormon og adrenokorticotropin hormon såvel som vasopressin viser sig inkonsekvent at være overproduceret ved depression, og dehydroepiandrosteron er fundet at være svækket; forholdet mellem kortisol og dehydroepiandrosteron kan være forhøjet som en relativt stabil markør i TRD, der vedvarer efter remission.109 Neuroendokrine hormondysfunktioner har længe været forbundet med depression, og hypothyroidisme kan også spille en årsagsrolle ved nedtrykt humør.110 Ydermere kan thyreoidearesponser normalisere med vellykket behandling af depression.111
Inden for ovenstående er det vigtigt også at overveje signalveje på tværs af systemer, såsom glykogensyntase kinase-3, mitogen-aktiveret proteinkinase og cyklisk adenosin 3?,5?-monophosphat, involveret i synaptisk plasticitet112 og modificeret af antidepressiva.113 Yderligere potentielle biomarkørkandidater, der især spænder over biologiske systemer, måles ved hjælp af neuroimaging eller genetik. Som reaktion på manglen på robuste og meningsfulde genomiske forskelle mellem deprimerede og ikke-deprimerede populationer, kunne 114 nye genetiske tilgange såsom polygene score115 eller telomer længde116,117 vise sig mere nyttige. Yderligere biomarkører, der vinder popularitet, er at undersøge cirkadiske cyklusser eller kronobiologiske biomarkører ved hjælp af forskellige kilder. Aktigrafi kan give en objektiv vurdering af søvn- og vågenaktivitet og hvile gennem et accelerometer, og aktigrafiske enheder kan i stigende grad måle yderligere faktorer såsom lyseksponering. Dette kan være mere nyttigt til påvisning end almindeligt anvendte subjektive rapporter om patienter og kunne give nye forudsigelser for behandlingsrespons.118 Spørgsmålet om, hvilke biomarkører der er de mest lovende til translationel brug, er et udfordrende spørgsmål, som uddybes nedenfor.
Nuværende udfordringer
For hvert af disse fem gennemgåede neurobiologiske systemer følger beviserne en lignende fortælling: der findes mange biomarkører, som i nogle henseender er forbundet med depression. Disse markører er ofte indbyrdes forbundne på en kompleks måde, der er svær at modellere. Evidensen er inkonsekvent, og det er sandsynligt, at nogle er epifænomener af andre faktorer, og nogle er kun vigtige hos en undergruppe af patienter. Biomarkører vil sandsynligvis være nyttige gennem en række forskellige veje (f.eks. dem, der forudsiger efterfølgende respons på behandlingen, dem, der indikerer, at specifikke behandlinger er mere tilbøjelige til at være effektive eller dem, der ændrer sig med interventioner uanset kliniske forbedringer). Nye metoder er nødvendige for at maksimere konsekvens og klinisk anvendelighed af biologiske vurderinger i psykiatriske populationer.
Biomarkørvariabilitet
Variation af biomarkører over tid og på tværs af situationer vedrører mere nogle typer (f.eks. proteomics) end andre (genomics). Standardiserede normer for mange eksisterer ikke eller er ikke blevet bredt accepteret. Faktisk afhænger indflydelsen af miljøfaktorer på markører ofte af genetisk sammensætning og andre fysiologiske forskelle mellem mennesker, som ikke alle kan forklares. Dette gør vurderingen af biomarkøraktivitet og identifikation af biologiske abnormiteter vanskelig at fortolke. På grund af antallet af potentielle biomarkører er mange ikke blevet målt bredt eller i et komplet panel sammen med andre relevante markører.
Mange faktorer er blevet rapporteret for at ændre proteinniveauerne på tværs af biologiske systemer hos patienter med affektive lidelser. Sammen med forskningsrelaterede faktorer såsom varighed og betingelser for opbevaring (som kan forårsage nedbrydning af nogle forbindelser), omfatter disse tidspunkt på dagen målt, etnicitet, motion,119 kost (f.eks. mikrobiomaktivitet, især forudsat at de fleste blodbiomarkørundersøgelser gør det ikke kræver en fasteprøve),120 rygning og stofbrug,121 samt helbredsfaktorer (såsom komorbide inflammatoriske, kardiovaskulære eller andre fysiske sygdomme). For eksempel, selvom forhøjet inflammation ses hos deprimerede, men ellers raske individer sammenlignet med ikke-depressive grupper, har deprimerede individer, som også har en komorbid immunrelateret tilstand, ofte endnu højere niveauer af cytokiner end dem uden depression eller sygdom.122 Nogle fremtrædende faktorer mht. sandsynlig involvering i forholdet mellem biomarkører, depression og behandlingsrespons er skitseret nedenfor.
Stress. Både endokrine og immunresponser har velkendte roller i at reagere på stress (fysiologisk eller psykologisk), og forbigående stress på tidspunktet for biologisk prøveindsamling måles sjældent i forskningsstudier på trods af variationen af denne faktor mellem individer, der kan accentueres af nuværende depressive symptomer. Både akutte og kroniske psykologiske stressfaktorer virker som en immunudfordring, der accentuerer inflammatoriske reaktioner på kort og længere sigt.123,124 Dette fund strækker sig til oplevelsen af stress i det tidlige liv, som er blevet forbundet med voksne inflammatoriske forhøjelser, der er uafhængige af stress oplevet som en voksen.125,126 Under traumatisk barndomsoplevelse er øget betændelse også kun blevet rapporteret hos de børn, der i øjeblikket var deprimerede.127 Omvendt kan personer med depression og en historie med barndomstraumer have sløvet kortisol-reaktioner på stress sammenlignet med dem med depression og ingen traumer i det tidlige liv.128 Stress-inducerede HPA-akseændringer ser ud til at være forbundet med kognitiv funktion,129 såvel som depressionssubtype eller variation i HPA-relaterede gener.130 Stress har også kort- og langsigtede hæmmende virkninger på neurogenese131 og andre neurale mekanismer.132 Det er uklart præcist, hvordan barndomstraumer påvirker biologiske markører hos deprimerede voksne s, men det er muligt, at stress tidligt i livet disponerer nogle individer for at udholde stressreaktioner i voksenalderen, som forstærkes psykologisk og/eller biologisk.
Kognitiv funktion. Neurokognitive dysfunktioner forekommer hyppigt hos mennesker med affektive lidelser, selv ved umedicineret MDD.133 Kognitive underskud forekommer kumulative sammen med behandlingsresistens.134 Neurobiologisk vil HPA-aksen129 og neurotrofiske systemer135 sandsynligvis spille en nøglerolle i dette forhold. Neurotransmittere noradrenalin og dopamin er sandsynligvis vigtige for kognitive processer såsom indlæring og hukommelse.136 Forhøjede inflammatoriske reaktioner er blevet forbundet med kognitiv tilbagegang og påvirker sandsynligvis kognitiv funktion i depressive episoder137 og i remission gennem en række forskellige mekanismer.138 Faktisk, Krogh et al139 foreslog, at CRP er tættere relateret til kognitiv præstation end til kernesymptomerne på depression.
Alder, køn og BMI. Fraværet eller tilstedeværelsen og retningen af biologiske forskelle mellem mænd og kvinder har været særligt varierende i beviserne til dato. Neuroendokrine hormonvariationer mellem mænd og kvinder interagerer med depressionsfølsomhed.140 En gennemgang af inflammationsundersøgelser rapporterede, at kontrol for alder og køn ikke påvirkede patientkontrolforskelle i inflammatoriske cytokiner (selvom sammenhængen mellem IL-6 og depression blev reduceret med alderen, hvilket stemmer overens med teorier om, at inflammation generelt stiger med alderen).41,141 VEGF-forskelle mellem patienter og kontroller er større i undersøgelser, der vurderer yngre prøver, mens køn, BMI og kliniske faktorer ikke påvirkede disse sammenligninger på et meta-analytisk niveau.77. manglen på justering for BMI i tidligere undersøgelser af inflammation og depression ser ud til at forvirre meget signifikante forskelle rapporteret mellem disse grupper.41 Forstørret fedtvæv er blevet definitivt påvist at stimulere cytokinproduktionen såvel som at være tæt forbundet med metaboliske markører.142 Fordi psykotrope lægemidler kan være forbundet med wei ght gain og et højere BMI, og disse har været forbundet med behandlingsresistens ved depression, er dette et vigtigt område at undersøge.
Medicin. Mange biomarkørundersøgelser i depression (både i tværsnit og på langs) har indsamlet baseline-prøver i umedicinerede deltagere for at reducere heterogenitet. Men mange af disse vurderinger er taget efter en udvaskningsperiode fra medicin, hvilket efterlader den potentielt betydelige forvirrende faktor med resterende ændringer i fysiologien, forværret af det omfattende udvalg af tilgængelige behandlinger, der kan have haft forskellige virkninger på inflammation. Nogle undersøgelser har udelukket psykotropisk, men ikke anden medicinbrug: Især er p-piller hyppigt tilladt hos forskningsdeltagere og ikke kontrolleret for i analyser, hvilket for nylig har vist sig at øge hormon- og cytokinniveauet.143,144 Adskillige undersøgelser indikerer, at antidepressivum medicin har virkninger på det inflammatoriske respons,34,43,49,145 147 HPA-akse,108 neurotransmitter,148 og neurotrofisk149 aktivitet. Imidlertid har de talrige potentielle behandlinger for depression distinkte og komplekse farmakologiske egenskaber, hvilket tyder på, at der kan være diskrete biologiske effekter af forskellige behandlingsmuligheder, understøttet af aktuelle data. Det er blevet teoretiseret, at ud over monoamin-effekter vil specifik serotonin-målrettet medicin (dvs. SSRI'er) sandsynligvis målrette Th2-skift i inflammation, og noradrenerge antidepressiva (f.eks. SNRI'er) bevirke et Th1-skift.150 Det er endnu ikke muligt at bestemme virkningen af individuelle eller kombinationsmedicin på biomarkører. Disse er sandsynligvis medieret af andre faktorer, herunder længden af behandlingen (få forsøg vurderer langvarig medicinbrug), prøvens heterogenitet og ikke stratificering af deltagere efter respons på behandlingen.
Heterogenitet
Metodisk. Som nævnt ovenfor er forskelle (mellem og inden for undersøgelser) med hensyn til hvilke behandlinger (og kombinationer), deltagerne tager og tidligere har taget, bundet til at introducere heterogenitet i forskningsresultater, især i biomarkørforskning. Ud over dette varierer mange andre design- og prøvekarakteristika på tværs af undersøgelser, hvilket øger vanskeligheden med at fortolke og tilskrive resultater. Disse omfatter måleparametre for biomarkører (f.eks. assay-sæt) og metoder til indsamling, opbevaring, behandling og analyse af markører i depression. Hiles et al141 undersøgte nogle kilder til inkonsistens i litteraturen om inflammation og fandt, at nøjagtigheden af depressionsdiagnose, BMI og komorbide sygdomme var vigtigst at tage højde for ved vurdering af perifer inflammation mellem deprimerede og ikke-deprimerede grupper.
Klinisk. Den omfattende heterogenitet af deprimerede befolkningsgrupper er veldokumenteret151 og er en kritisk bidragyder til kontrasterende resultater inden for forskningslitteraturen. Det er sandsynligt, at selv inden for diagnoser er unormale biologiske profiler begrænset til undergrupper af individer, som muligvis ikke er stabile over tid. Sammenhængende undergrupper af mennesker, der lider af depression, kan identificeres gennem en kombination af psykologiske og biologiske faktorer. Nedenfor skitserer vi potentialet for at udforske undergrupper for at møde de udfordringer, som biomarkørvariabilitet og heterogenitet udgør.
Undertyper indenfor depression
Hidtil har ingen homogene undergrupper inden for depressionsepisoder eller lidelser været pålideligt i stand til at skelne mellem patienter baseret på symptompræsentationer eller behandlingsrespons.152 Eksistensen af en undergruppe, hvor biologiske aberrationer er mere udtalte, ville bidrage til at forklare heterogeniteten mellem tidligere undersøgelser og kunne katalysere vejen mod stratificeret behandling. Kunugi et al153 har foreslået et sæt af fire potentielle undertyper baseret på rollen af forskellige neurobiologiske systemer, der viser klinisk relevante undertyper i depression: dem med hypercortisolisme, der viser sig med melankolsk depression, eller hypokortisolisme, der afspejler en atypisk undertype, en dopaminrelateret undergruppe af patienter, som evt. forekommer fremtrædende med anhedoni (og kunne reagere godt på f.eks. aripiprazol) og en inflammatorisk undertype karakteriseret ved forhøjet inflammation. Mange artikler, der fokuserer på inflammation, har specificeret sagen for eksistensen af en "inflammatorisk subtype" inden for depression.55,56,154,155 Kliniske korrelater af forhøjet inflammation er endnu ikke fastlagt, og få direkte forsøg er blevet gjort på at opdage, hvilke deltagere der kan omfatte denne kohorte. Det er blevet foreslået, at personer med atypisk depression kunne have højere niveauer af inflammation end den melankolske subtype156, hvilket måske ikke er i overensstemmelse med resultaterne vedrørende HPA-aksen i melankolske og atypiske subtyper af depression. TRD37 eller depression med fremtrædende somatiske symptomer157 er også blevet anført som en potentiel inflammatorisk undertype, men neurovegetative (søvn, appetit, tab af libido), humør (herunder lavt humør, suicidalitet og irritabilitet) og kognitive symptomer (herunder affektiv bias og skyldfølelse)158 alle synes relateret til biologiske profiler. Yderligere potentielle kandidater til en inflammatorisk undertype involverer oplevelsen af sygdomsadfærdslignende symptomer159,160 eller et metabolisk syndrom.158
Tilbøjeligheden til (hypo) mani kan skelne biologisk mellem patienter, der lider af depression. Beviser tyder nu på, at bipolære sygdomme er en mangefacetteret gruppe af stemningslidelser, hvor bipolar subsyndromal lidelse findes mere udbredt end tidligere anerkendt.161 Unøjagtig og/eller forsinket påvisning af bipolar lidelse er for nylig blevet fremhævet som et stort problem i klinisk psykiatri, med Den gennemsnitlige tid til at korrigere diagnosen overstiger ofte et årti162, og denne forsinkelse forårsager større sværhedsgrad og omkostninger ved den samlede sygdom.163 Med størstedelen af patienter med bipolar lidelse, der indledningsvis præsenterede en eller flere depressive episoder, og unipolar depression er den hyppigste fejldiagnose, faktorer, der kan skelne mellem unipolar og bipolar depression, har væsentlige implikationer.164 Bipolære spektrumforstyrrelser er sandsynligvis blevet uopdaget i nogle tidligere MDD-biomarkørundersøgelser, og mangel på bevis har indikeret differentiering af HPA-akseaktivitet109 eller inflammation165,166 mellem bipolar og unipolar depr session. Disse sammenligninger er imidlertid sparsomme, har små stikprøvestørrelser, identificerede ikke-signifikante trendeffekter eller rekrutterede populationer, der ikke var godt karakteriseret ved diagnose. Disse undersøgelser undersøger heller ikke, hvilken rolle behandlingsreaktivitet spiller i disse relationer.
Både bipolære lidelser167 og behandlingsresistens168 er ikke dikotomiske konstruktioner og ligger på kontinua, hvilket øger udfordringen med subtypeidentifikation. Udover subtypebestemmelse er det værd at bemærke, at mange biologiske abnormiteter observeret ved depression på samme måde findes hos patienter med andre diagnoser. Transdiagnostiske undersøgelser er således også potentielt vigtige.
Udfordringer til måling af biomarkører
Biomarkør valg. Det store antal potentielt nyttige biomarkører udgør en udfordring for psykobiologien med at afgøre, hvilke markører der er impliceret på hvilken måde og for hvem. For at øge udfordringen har relativt få af disse biomarkører været genstand for tilstrækkelig undersøgelse i depression, og for de fleste er deres præcise roller i raske og kliniske populationer ikke godt forstået. På trods af dette er der gjort en række forsøg på at foreslå lovende biomarkørpaneler. Ud over Brand et al.s 16 sæt markører med stærkt potentiale27 skitserer Lopresti et al. et yderligere omfattende sæt oxidative stressmarkører med potentiale til at forbedre behandlingsrespons.28 Papakostas et al definerede a priori et sæt på ni serummarkører biologiske systemer (BDNF, cortisol, opløselig TNFa-receptor type II, alpha1-antitrypsin, apolipoprotein CIII, epidermal vækstfaktor, myeloperoxidase, prolactin og resistin) i validerings- og replikationsprøver med MDD. Når de først var kombineret, var et sammensat mål for disse niveauer i stand til at skelne mellem MDD og kontrolgrupper med 80 %–90 % nøjagtighed.169 Vi foreslår, at selv disse ikke dækker alle potentielle kandidater inden for dette felt; se tabel 2 for en ikke-udtømmende afgrænsning af biomarkører med potentiale for depression, indeholdende både dem med en evidensbase og lovende nye markører.
Teknologi. På grund af teknologiske fremskridt er det nu muligt (faktisk bekvemt) at måle et stort udvalg af biomarkører samtidigt til en lavere pris og med højere følsomhed, end det har været tilfældet tidligere. På nuværende tidspunkt er denne evne til at måle adskillige forbindelser forud for vores evne til effektivt at analysere og fortolke dataene,170 noget, der vil fortsætte med stigningen i biomarkørarrays og nye markører, såsom med metabolomics. Dette skyldes i høj grad en mangel på forståelse for de præcise roller af og de indbyrdes sammenhænge mellem markører, og en utilstrækkelig forståelse af, hvordan relaterede markører associerer på tværs af forskellige biologiske niveauer (f.eks. genetisk, transkription, protein) inden for og mellem individer. Big data ved hjælp af nye analytiske tilgange og standarder vil hjælpe med at løse dette, og nye metoder bliver foreslået; et eksempel er udviklingen af en statistisk tilgang baseret på flux-baseret analyse for at opdage nye potentielle metaboliske markører baseret på deres reaktioner mellem netværk og integrere genekspression med metabolitdata.171 Maskinlæringsteknikker bliver allerede anvendt og vil hjælpe med modeller, der bruger biomarkører data til at forudsige behandlingsresultater i undersøgelser med big data.172
Aggregerende biomarkører. At undersøge en række biomarkører samtidigt er et alternativ til at inspicere isolerede markører, der kunne give et mere præcist synspunkt ind i det komplekse net af biologiske systemer eller netværk.26 Også for at hjælpe med at fjerne modstridende beviser i denne litteratur til dato (især hvor biomarkør netværk og interaktioner er godt forstået), kan biomarkørdata derefter aggregeres eller indekseres. En udfordring er at identificere den optimale metode til at udføre dette, og det kan kræve forbedringer i teknologi og/eller nye analytiske teknikker (se afsnittet "Big data"). Historisk set har forhold mellem to forskellige biomarkører givet interessante resultater.109,173 Der er gjort få forsøg på at aggregere biomarkørdata i større skala, såsom dem, der anvender principal komponentanalyse af proinflammatoriske cytokinnetværk.174 I en meta-analyse er proinflammatoriske cytokiner blevet konverteret til en enkelt-effekt størrelsesscore for hver undersøgelse og viste samlet set signifikant højere inflammation før antidepressiv behandling, hvilket forudsagde efterfølgende manglende respons i ambulante undersøgelser. Sammensatte biomarkørpaneler er både en udfordring og mulighed for fremtidig forskning for at identificere meningsfulde og pålidelige resultater, der kan anvendes til at forbedre behandlingsresultater.43 En undersøgelse foretaget af Papakostas et al. tog en alternativ tilgang, idet de udvalgte et panel af heterogene serumbiomarkører (af inflammatoriske, HPA-akse og metaboliske systemer), som var blevet indiceret til at være forskellige mellem deprimerede og kontrolpersoner i en tidligere undersøgelse og sammensatte disse til en risikoscore, som var forskellig i to uafhængige prøver og en kontrolgruppe med >80 % sensitivitet og specificitet.169
Big data. Brugen af big data er sandsynligvis nødvendig for at løse de aktuelle udfordringer, der er skitseret omkring heterogenitet, biomarkørvariabilitet, identifikation af de optimale markører og bringe feltet mod translationel, anvendt forskning i depression. Men som skitseret ovenfor bringer dette teknologiske og videnskabelige udfordringer.175 Sundhedsvidenskaben er først for nylig begyndt at bruge big data-analyse, et årti eller deromkring senere end i erhvervslivet. Undersøgelser som iSPOT-D152 og konsortier som Psychiatric Genetics Consortium176 skrider dog frem med vores forståelse af biologiske mekanismer i psykiatrien. Maskinlæringsalgoritmer er i meget få undersøgelser begyndt at blive anvendt på biomarkører for depression: en nylig undersøgelse samlede data fra >5,000 deltagere af 250 biomarkører; efter multiple imputation af data blev der udført en maskinlæringsboostet regression, hvilket indikerede 21 potentielle biomarkører. Efter yderligere regressionsanalyser blev tre biomarkører udvalgt som stærkest associeret med depressive symptomer (højt varierende røde blodlegemer, serumglukose og bilirubinniveauer). Forfatterne konkluderer, at big data kan bruges effektivt til at generere hypoteser.177 Større biomarkørfænotypeprojekter er nu i gang og vil hjælpe med at fremme vores rejse ind i fremtiden for neurobiologien af depression.
Fremtidsudsigter
Identifikation af biomarkørpanel
Resultaterne i litteraturen til dato kræver replikation i store undersøgelser. Dette gælder især for nye biomarkører, såsom kemokin thymus og aktiveringsreguleret kemokin og vækstfaktoren tyrosinkinase 2, som, så vidt vi ved, ikke er blevet undersøgt i klinisk deprimerede og sunde kontrolprøver. Big data-undersøgelser skal analysere omfattende biomarkørpaneler og bruge sofistikerede analyseteknikker til fuldt ud at fastslå forholdet mellem markører og de faktorer, der ændrer dem i kliniske og ikke-kliniske populationer. Derudover kan storskala replikationer af hovedkomponentanalyse etablere stærkt korrelerede grupper af biomarkører og kunne også informere brugen af "kompositter" i biologisk psykiatri, hvilket kan øge homogeniteten af fremtidige fund.
Opdagelse af homogene undertyper
Med hensyn til valg af biomarkør kan der være behov for flere paneler for forskellige potentielle veje, som forskning kunne implicere. Samlet set indikerer den nuværende evidens, at biomarkørprofiler er sikkert, men abstrueret ændret i en underpopulation af individer, der i øjeblikket lider af depression. Dette kan etableres inden for eller på tværs af diagnostiske kategorier, hvilket vil forklare en vis inkonsistens i de fund, der kan observeres i denne litteratur. Kvantificering af en biologisk undergruppe (eller undergrupper) kan mest effektivt lettes ved en stor klyngeanalyse af biomarkørnetværkspaneler i depression. Dette ville illustrere variation inden for populationen; latente klasseanalyser kunne udvise distinkte kliniske karakteristika baseret på for eksempel inflammation.
Specifikke behandlingseffekter på inflammation og respons
Alle almindeligt ordinerede behandlinger for depression bør vurderes grundigt for deres specifikke biologiske virkninger, også tage højde for effektiviteten af behandlingsforsøg. Dette kan gøre det muligt for konstruktioner relateret til biomarkører og symptompræsentationer at forudsige resultater af en række antidepressive behandlinger på en mere personlig måde og kan være muligt i forbindelse med både unipolar og bipolar depression. Dette vil sandsynligvis være nyttigt for nye potentielle behandlinger såvel som aktuelt indikerede behandlinger.
Prospektiv bestemmelse af behandlingsrespons
Anvendelse af ovenstående teknikker vil sandsynligvis resultere i en forbedret evne til at forudsige behandlingsresistens prospektivt. Mere autentiske og vedvarende (f.eks. langsigtede) målinger af behandlingsrespons kan bidrage til dette. Vurdering af andre valide mål for patientens velbefindende (såsom livskvalitet og hverdagsfunktion) kunne give en mere holistisk vurdering af behandlingsresultater, der kan forbindes tættere med biomarkører. Mens biologisk aktivitet alene muligvis ikke er i stand til at skelne behandlingsrespondere fra non-responders, kan samtidig måling af biomarkører med psykosociale eller demografiske variable integreres med biomarkørinformation i udviklingen af en prædiktiv model for utilstrækkelig behandlingsrespons. Hvis en pålidelig model udvikles til at forudsige respons (enten for den deprimerede befolkning eller en subpopulation) og valideres retrospektivt, kan et translationelt design fastslå dets anvendelighed i et stort kontrolleret forsøg.
Mod stratificerede behandlinger
På nuværende tidspunkt er patienter med depression ikke systematisk henvist til at modtage et optimeret interventionsprogram. Hvis det er valideret, kan et stratificeret forsøgsdesign anvendes til at teste en model til at forudsige manglende respons og/eller for at bestemme, hvor en patient skal triageres i en trinvis plejemodel. Dette kan være nyttigt i både standardiserede og naturalistiske behandlingsindstillinger på tværs af forskellige typer intervention. I sidste ende kan der udvikles en klinisk levedygtig model for at give individer den mest passende behandling, for at genkende dem, der sandsynligvis vil udvikle refraktær depression, og give forbedret pleje og overvågning til disse patienter. Patienter identificeret som værende i risiko for behandlingsresistens kan få ordineret en samtidig psykologisk og farmakologisk behandling eller kombinationsfarmakoterapi. Som et spekulativt eksempel kan deltagere uden proinflammatoriske cytokinforhøjelser være indiceret til at modtage psykologisk snarere end farmakologisk terapi, mens en undergruppe af patienter med særlig høj inflammation kunne modtage et antiinflammatorisk middel som supplement til standardbehandling. I lighed med stratificering kan personaliserede behandlingsudvælgelsesstrategier være mulige i fremtiden. For eksempel kan et særligt deprimeret individ have markant høj TNF? niveauer, men ingen andre biologiske abnormiteter, og kunne drage fordel af kortvarig behandling med en TNF? antagonist.54 Personlig behandling kan også indebære monitorering af biomarkørekspression under behandlingen for at informere om mulige interventionsændringer, længden af den nødvendige fortsatte terapi eller for at opdage tidlige markører for tilbagefald.
Nye behandlingsmål
Der er et stort antal potentielle behandlinger, der kan være effektive mod depression, som ikke er blevet tilstrækkeligt undersøgt, herunder nye eller genbrugte interventioner fra andre medicinske discipliner. Nogle af de mest populære mål har været i anti-inflammatorisk medicin såsom celecoxib (og andre cyclooxygenase-2-hæmmere), TNF? antagonister etanercept og infliximab, minocyclin eller aspirin. Disse virker lovende.178 Antiglukokortikoidforbindelser, herunder ketoconazol179 og metyrapone,180 er blevet undersøgt for depression, men begge har ulemper med deres bivirkningsprofil, og det kliniske potentiale af metyrapon er usikkert. Mifepriston181 og kortikosteroiderne fludrocortison og spironolacton,182 og dexamethason og hydrocortison183 kan også være effektive til behandling af depression på kort sigt. Målretning mod glutamat-N-methyl-d-aspartat-receptorantagonister, herunder ketamin, kan repræsentere effektive behandlinger ved depression.184 Omega-3 flerumættede fedtsyrer påvirker inflammatorisk og metabolisk aktivitet og ser ud til at vise en vis effektivitet mod depression.185 Det er muligt, at statiner kan har antidepressive virkninger186 gennem relevante neurobiologiske veje.187
På denne måde er de biokemiske virkninger af antidepressiva (se afsnittet Medikamenter ) blevet udnyttet til kliniske fordele inden for andre discipliner: især gastroenterologiske, neurologiske og uspecifikke symptomsygdomme.188 Anti-inflammatoriske virkninger af antidepressiva kan udgøre en del af mekanismen for disse fordele. Lithium er også blevet foreslået at reducere inflammation, kritisk gennem glykogensyntase-kinase-3-veje.189 Et fokus på disse effekter kan vise sig at være informativt for en depressionsbiomarkørsignatur, og biomarkører kan igen repræsentere surrogatmarkører for udvikling af nye lægemidler.

Dr. Alex Jimenez's Insight
Depression er en psykisk lidelse karakteriseret ved alvorlige symptomer, som påvirker humøret, herunder tab af interesse for aktiviteter. Nyere forskningsundersøgelser har dog fundet ud af, at det kan være muligt at diagnosticere depression ved hjælp af mere end blot en patients adfærdssymptomer. Ifølge forskerne er identifikation af let tilgængelige biomarkører, som kan diagnosticere depression mere præcist, grundlæggende for at forbedre en patients generelle sundhed og velvære. For eksempel tyder kliniske fund på, at personer med svær depressiv lidelse eller MDD har lavere niveauer af molekylet acetyl-L-carnitin eller LAC i deres blod end raske kontroller. I sidste ende kan etablering af biomarkører for depression potentielt hjælpe med bedre at bestemme, hvem der er i risiko for at udvikle lidelsen, samt hjælpe sundhedspersonale med at bestemme den bedste behandlingsmulighed for en patient med depression.
Konklusion
Litteraturen indikerer, at cirka to tredjedele af patienter med depression ikke opnår remission til en indledende behandling, og at sandsynligheden for manglende respons stiger med antallet af afprøvede behandlinger. Tilvejebringelse af ineffektive terapier har væsentlige konsekvenser for individuelle og samfundsmæssige omkostninger, herunder vedvarende nød og dårligt velbefindende, risiko for selvmord, tab af produktivitet og spildte sundhedsressourcer. Den store litteratur om depression indikerer et stort antal biomarkører med potentiale til at forbedre behandlingen af mennesker med depression. Ud over neurotransmitter og neuroendokrine markører, som har været genstand for udbredt undersøgelse i mange årtier, fremhæver nyere indsigter den inflammatoriske respons (og immunsystemet mere generelt), metaboliske og vækstfaktorer som vigtige involverede i depression. Imidlertid viser overdreven kontrasterende beviser, at der er en række udfordringer, der skal tackles, før biomarkørforskning kan anvendes for at forbedre håndteringen og plejen af mennesker med depression. På grund af den rene kompleksitet af biologiske systemer, er samtidige undersøgelser af en omfattende række af markører i store prøver af betydelig fordel ved at opdage interaktioner mellem biologiske og psykologiske tilstande på tværs af individer. Optimering af måling af både neurobiologiske parametre og kliniske mål for depression vil sandsynligvis lette større forståelse. Denne gennemgang fremhæver også vigtigheden af at undersøge potentielt modificerende faktorer (såsom sygdom, alder, kognition og medicin) for at opnå en sammenhængende forståelse af depressionens biologi og mekanismer for behandlingsresistens. Det er sandsynligt, at nogle markører vil vise mest lovende for at forudsige behandlingsrespons eller modstand mod specifikke behandlinger i en undergruppe af patienter, og den samtidige måling af biologiske og psykologiske data kan øge evnen til prospektivt at identificere dem, der er i risiko for dårlige behandlingsresultater. Etablering af et biomarkørpanel har betydning for at øge diagnostisk nøjagtighed og prognose, såvel som for individualisering af behandlinger på det tidligst mulige stadie af depressiv sygdom og udvikling af effektive nye behandlingsmål. Disse implikationer kan være begrænset til undergrupper af deprimerede patienter. Vejene mod disse muligheder supplerer nyere forskningsstrategier for at knytte kliniske syndromer tættere til underliggende neurobiologiske substrater.6 Ud over at reducere heterogenitet kan dette lette et skift i retning af paritet af agtelse mellem fysisk og mental sundhed. Det er klart, at selv om der er behov for meget arbejde, har etablering af forholdet mellem relevante biomarkører og depressive lidelser væsentlige konsekvenser for at reducere byrden af depression på individuelt og samfundsmæssigt niveau.
Tak
Denne rapport repræsenterer uafhængig forskning finansieret af National Institute for Health Research (NIHR) Biomedical Research Center i South London og Maudsley NHS Foundation Trust og King's College London. De udtrykte synspunkter er forfatternes og ikke nødvendigvis dem fra NHS, NIHR eller sundhedsministeriet.
Fodnoter
Afsløring. AHY har i de sidste 3 år modtaget honorar for at tale fra Astra Zeneca (AZ), Lundbeck, Eli Lilly, Sunovion; honorar for rådgivning fra Allergan, Livanova og Lundbeck, Sunovion, Janssen; og forskningsstøtte fra Janssen og britiske finansieringsbureauer (NIHR, MRC, Wellcome Trust). AJC har i de sidste 3 år modtaget honorar for at tale fra Astra Zeneca (AZ), honorar for rådgivning fra Allergan, Livanova og Lundbeck og støtte til forskningsbevillinger fra Lundbeck og britiske finansieringsbureauer (NIHR, MRC, Wellcome Trust).
Forfatterne rapporterer ingen andre interessekonflikter i dette arbejde.
AfslutningsvisSelvom adskillige forskningsstudier har fundet hundredvis af biomarkører for depression, er der ikke mange, der har fastslået deres rolle i depressiv sygdom, eller hvordan nøjagtig biologisk information kunne bruges til at forbedre diagnose, behandling og prognose. Imidlertid gennemgår artiklen ovenfor den tilgængelige litteratur om de biomarkører, der er involveret under andre processer, og sammenligner de kliniske resultater med depression. Desuden kan nye fund om biomarkører for depression hjælpe med en bedre diagnosticering af depression for at følge op med bedre behandling. Oplysninger refereret fra National Center for Biotechnology Information (NCBI).�Omfanget af vores information er begrænset til kiropraktik såvel som til rygmarvsskader og -tilstande. For at diskutere emnet, er du velkommen til at spørge Dr. Jimenez eller kontakte os på�915-850-0900 .
Kurateret af Dr. Alex Jimenez
Yderligere emner: Rygsmerter
Rygsmerte er en af de mest udbredte årsager til handicap og savnede dage på arbejdspladsen over hele verden. Faktisk er rygsmerter blevet tilskrevet som den næst mest almindelige årsag til doktorkontorbesøg, der kun overstiger luftvejsinfektioner. Ca. 80 procent af befolkningen vil opleve en form for rygsmerter mindst én gang i hele deres liv. Ryggraden er en kompleks struktur bestående af knogler, led, ledbånd og muskler, blandt andet blødt væv. På grund af dette skader og / eller forværrede forhold, som f.eks herniated diske, kan i sidste ende føre til symptomer på rygsmerter. Sportsskader eller personskader er ofte den hyppigste årsag til rygsmerter, men nogle gange kan de enkleste bevægelser have smertefulde resultater. Heldigvis kan alternative behandlingsmuligheder, såsom kiropraktisk pleje, hjælpe lindring af rygsmerter ved brug af rygtilpasninger og manuelle manipulationer, der i sidste ende forbedrer smertelindring.

EKSTRA VIGTIG TEMNE: Håndtering af lænderygsmerter
FLERE EMNER: EKSTRA EKSTRA:�Kroniske smerter og behandlinger
Blank
Referencer
Luk harmonika
Oplysningerne heri om "Biomarkørernes rolle for depression" er ikke beregnet til at erstatte et en-til-en-forhold med en kvalificeret sundhedsperson eller autoriseret læge og er ikke medicinsk rådgivning. Vi opfordrer dig til at træffe sundhedsbeslutninger baseret på din forskning og partnerskab med en kvalificeret sundhedsperson.
Bloginformation og diskussioner om omfang
Vores informationsomfang er begrænset til kiropraktik, muskuloskeletal, fysisk medicin, wellness, bidragende ætiologisk viscerosomatiske forstyrrelser inden for kliniske præsentationer, tilhørende somatovisceral refleks klinisk dynamik, subluksationskomplekser, følsomme helbredsproblemer og/eller funktionel medicin artikler, emner og diskussioner.
Vi giver og præsenterer klinisk samarbejde med specialister fra forskellige discipliner. Hver specialist er styret af deres faglige omfang af praksis og deres licensjurisdiktion. Vi bruger funktionelle sundheds- og velværeprotokoller til at behandle og understøtte pleje af skader eller lidelser i bevægeapparatet.
Vores videoer, indlæg, emner, emner og indsigt dækker kliniske forhold, problemstillinger og emner, der relaterer til og direkte eller indirekte understøtter vores kliniske anvendelsesområde.*
Vores kontor har med rimelighed forsøgt at give støttende citater og har identificeret den eller de relevante forskningsundersøgelser, der understøtter vores indlæg. Vi leverer kopier af understøttende forskningsundersøgelser tilgængelige for tilsynsråd og offentligheden efter anmodning.
Vi forstår, at vi dækker forhold, der kræver yderligere forklaring på, hvordan det kan hjælpe med en bestemt plejeplan eller behandlingsprotokol. derfor er du velkommen til at spørge for yderligere at diskutere emnet ovenfor Dr. Alex Jimenez, DC, eller kontakte os på 915-850-0900.
Vi er her for at hjælpe dig og din familie.
Blessings
Dr. Alex Jimenez A.D. MSACP, RN*, CCST, Ifmcp*, CIFM*, ATN*
Email: coach@elpasofunctionalmedicine.com
Licenseret som Doctor of Chiropractic (DC) i Texas & New Mexico*
Texas DC-licensnummer TX5807, New Mexico DC Licensnr. NM-DC2182
Licenseret som registreret sygeplejerske (RN*) in Florida
Florida-licens RN-licens # RN9617241 (Kontrol nr. 3558029)
Kompakt status: Multi-State Licens: Bemyndiget til at praktisere i 40 stater*
Dr. Alex Jimenez DC, MSACP, RN*CIFM*, IFMCP*, ATN*, CCST
Mit digitale visitkort